
近日,中国药物临床试验登记与信息公示平台显示,礼来启动了一项国际多中心、随机、双盲、安慰剂对照III期研究(登记号:CTR20230785),旨在评估remternetug静脉输注治疗具有脑淀粉样蛋白和tau蛋白病理的早期症状性阿尔茨海默病(AD)受试者中的安全性和有效性。
该研究计划国内入组140人,国际入组1300人。受试者随机分组接受remternetug和生理盐水静脉滴注治疗,每12周注射1次,共计给药3个周期。主要终点是治疗76周后,至少1个人群的iADRS评分相比基线的变化。
阿尔茨海默症是一种主要发生于老年人的神经退行性疾病,临床特征是记忆障碍、失语、失用、失认、视空间技能损害、执行功能障碍以及人格和行为改变等全面性痴呆表现。统计数据显示,截至2019年底,中国阿尔茨海默症患者人数超1300万例,预计这一数字仍将逐年扩增。中国AD的患病率、死亡率均高于全球平均水平,且女性人群相关数据高于男性。
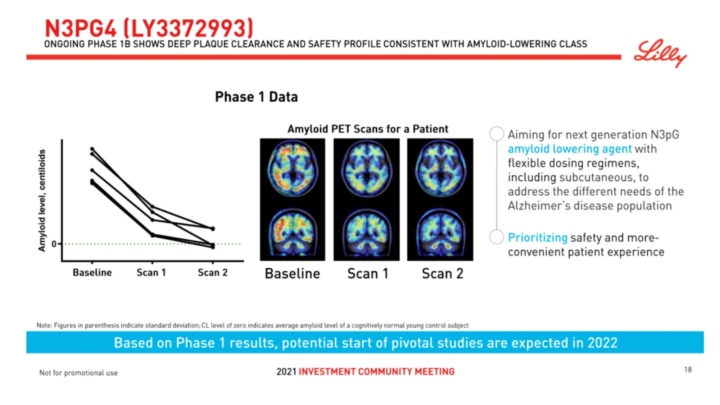
礼来表示,remternetug是donanemab的后续产品,属于“下一代抗淀粉样蛋白抗体”。Ib期临床研究显示,remternetug表现出深度斑块清除能力,并拥有良好的安全性。本次静脉输注III期研究中,用药时程为单次给药,12周为一个给药周期,共给药3个周期。
2月22日,礼来启动了一项remternetug皮下注射治疗早期症状性AD患者的III期临床试验(登记号:CTR20230358),两项研究拟在国内入组140例AD患者,国际入组1300例患者。
本文章来源于医药魔方Info,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们
