山东省临床肿瘤学会妇科肿瘤专家委员会成立大会暨第一次学术会议
手术原则
对于卵巢癌的治疗,手术是卵巢癌治疗的基础,对于早期的患者进行彻底的分期手术,包括彻底的盆腹腔探查、腹水冲洗液或腹水细胞学检查、腹膜多点活检、子宫双附件的切除、手术中避免肿瘤破裂、大网膜的切除和淋巴结的切除。对于晚期患者,最大程度地进行肿瘤细胞减灭术,尽可能地切除肉眼可见的病灶,满意减瘤术标准为残余肿瘤病灶直径<1cm,最好能达到没有肉眼可见的病灶。切除能够切除的肿大或可疑淋巴结,临床阴性的淋巴结不需要切除。为达满意的减瘤术,可根据需要切除部分肠管、阑尾、脾脏、胆囊、部分膀胱等。
特殊情况有如下几种:
希望保留生育功能的早期患者或者低风险恶性肿瘤(早期上皮性卵出癌、低度恶性潜能肿痛、生殖细胞肿瘤或恶性性索间质细胞瘤)可行保留生育功能手术。有临床指征建议转诊至生殖内分泌专家进行咨询评估。需进行全面的手术分期以排除更晚期疾病。明确的儿童/青春期及青年早期生殖细胞肿瘤可参照相关指南不行全面分期。
黏液性肿瘤:原发卵巢漫润性黏液肿瘤少见。须对上下消化道进行全面评估以排除转移。怀疑或确诊黏液性卵巢肿痛的患者需切除外观异常的阑尾。正常阑尾不须切除。若术中快速病理证实黏液性肿瘤且无可疑淋巴结,可不行淋巴结切除术
为什么要强调晚期肿瘤要进行满意的肿瘤细胞减灭术,因为满意的肿瘤细胞减灭术可改善患者的生存期,满意减灭术每增加10%,中位生存时间增加5.5%(下图)。如果手术达到,患者的OS、PFS较达到MR的患者长(下图)。
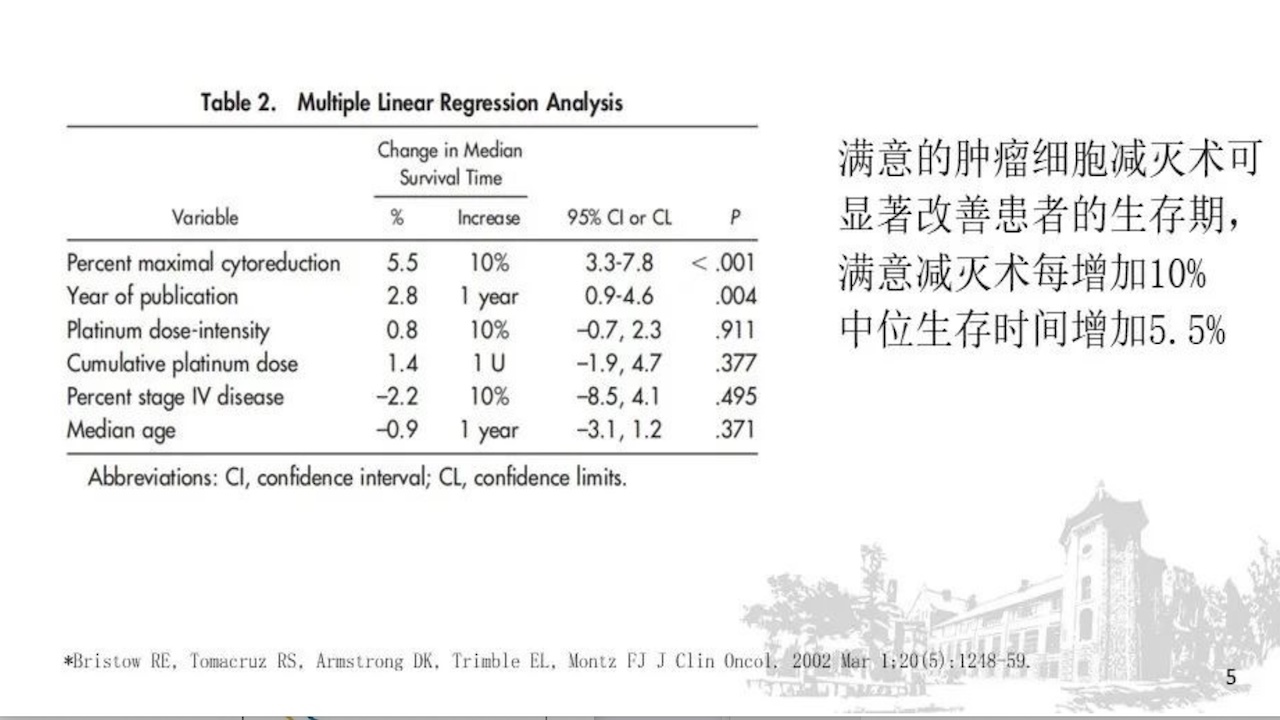
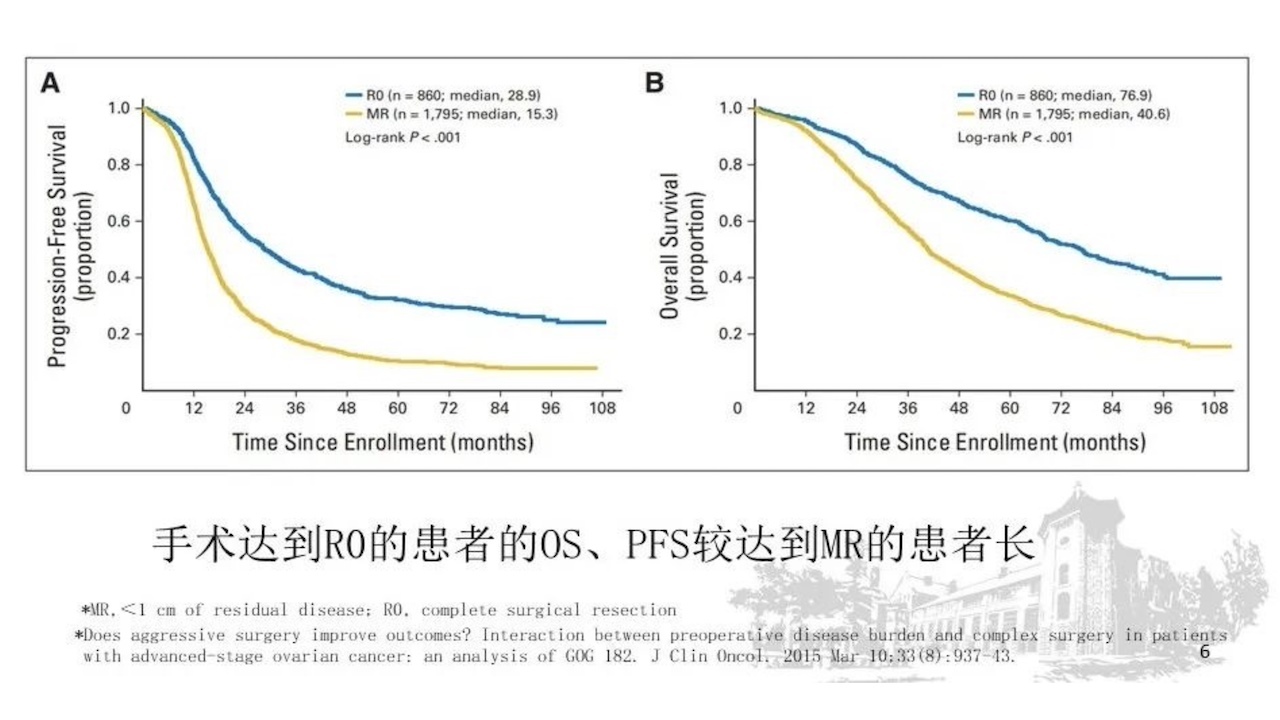
但是晚期卵巢癌患者预后受到多种因素的影响,卵巢癌的手术是越大越好吗?我们看一下手术并发症:局限在盆腔的手术:3-4级并发症发生率为5%;超根治手术:3-4级并发症发生率>20%;肠道手术明显增加围手术期的30天并发症发生率。下图所示,发生肠瘘的患者中接受RSR伴LBR者的比例高于无肠瘘的患者。
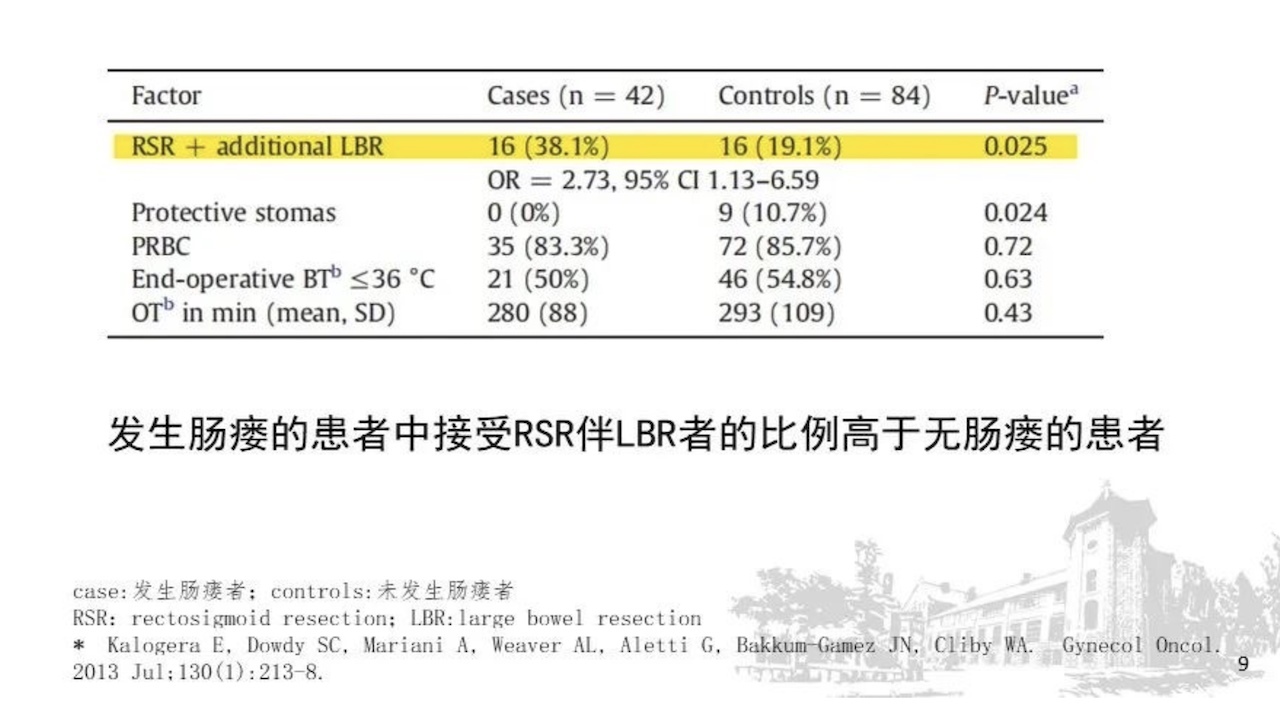
而且肠道手术并发症的升高可能直接或间接地通过延迟后续化疗抵消了R0手术带来的生存获益。
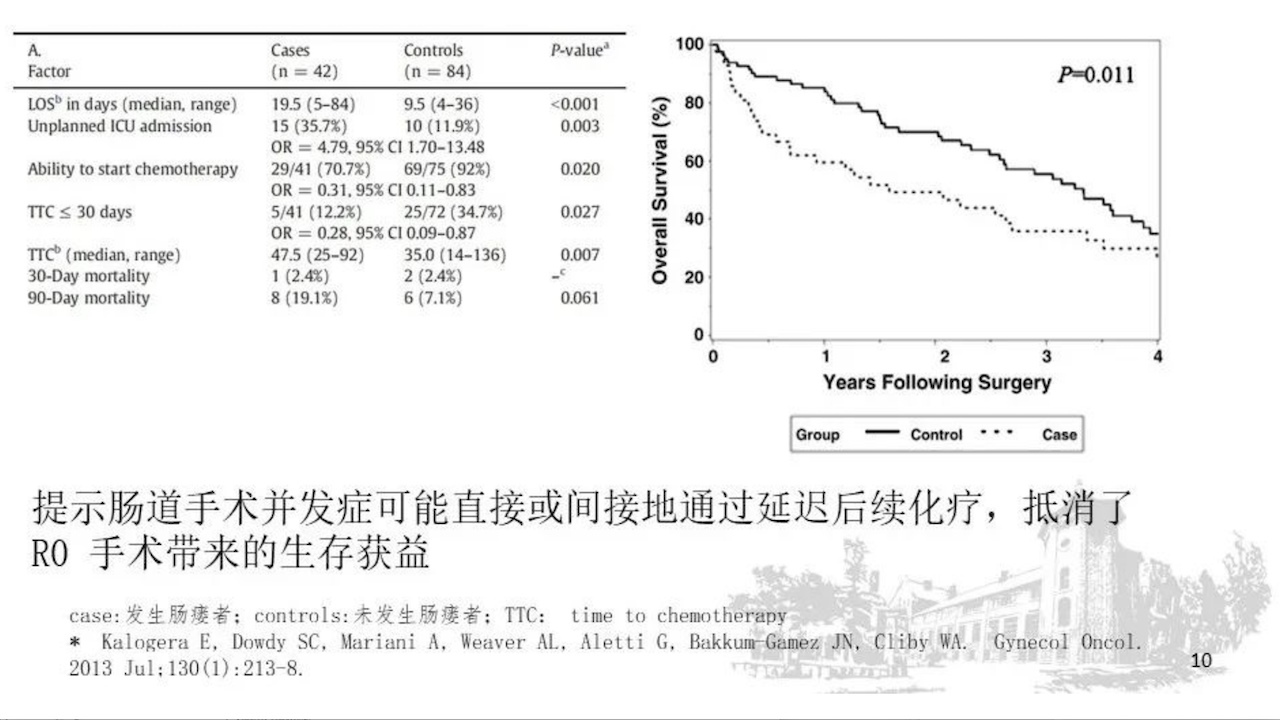
对于需要进行两个或两个以上器官切除以获得R0的肿瘤高负荷患者的预后明显差于其他患者,且切除器官数越多者预后越差。
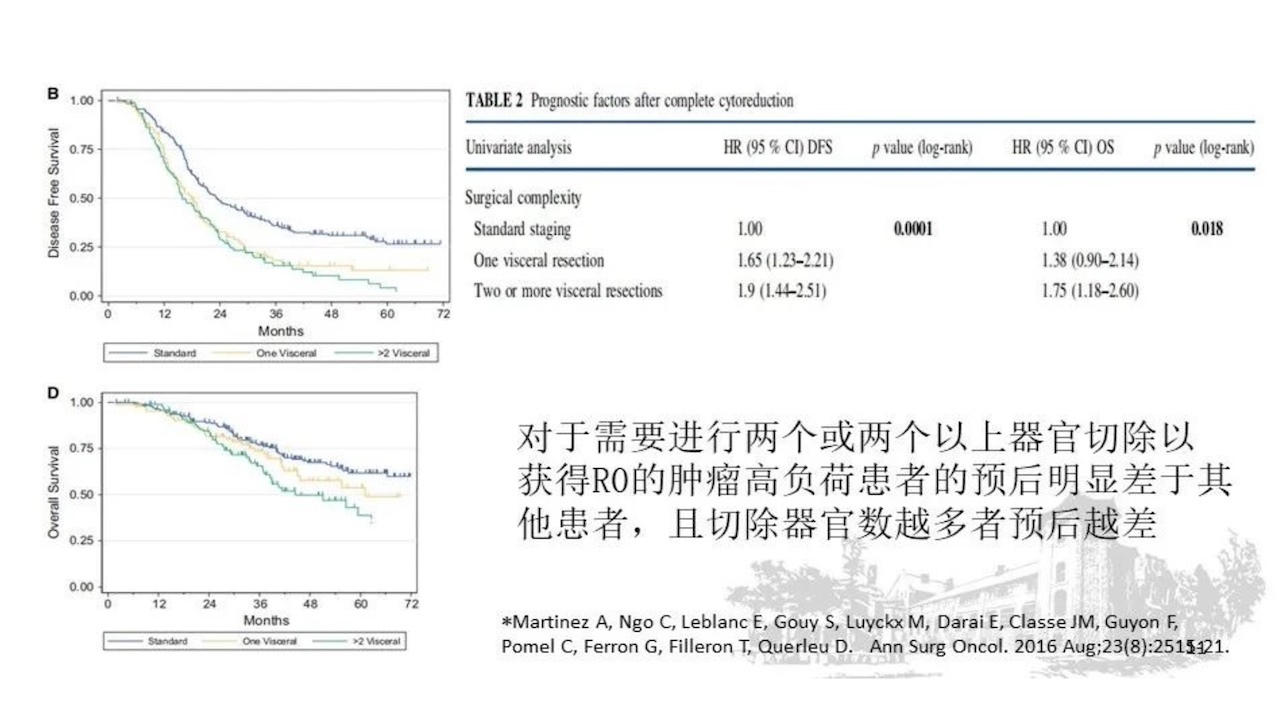
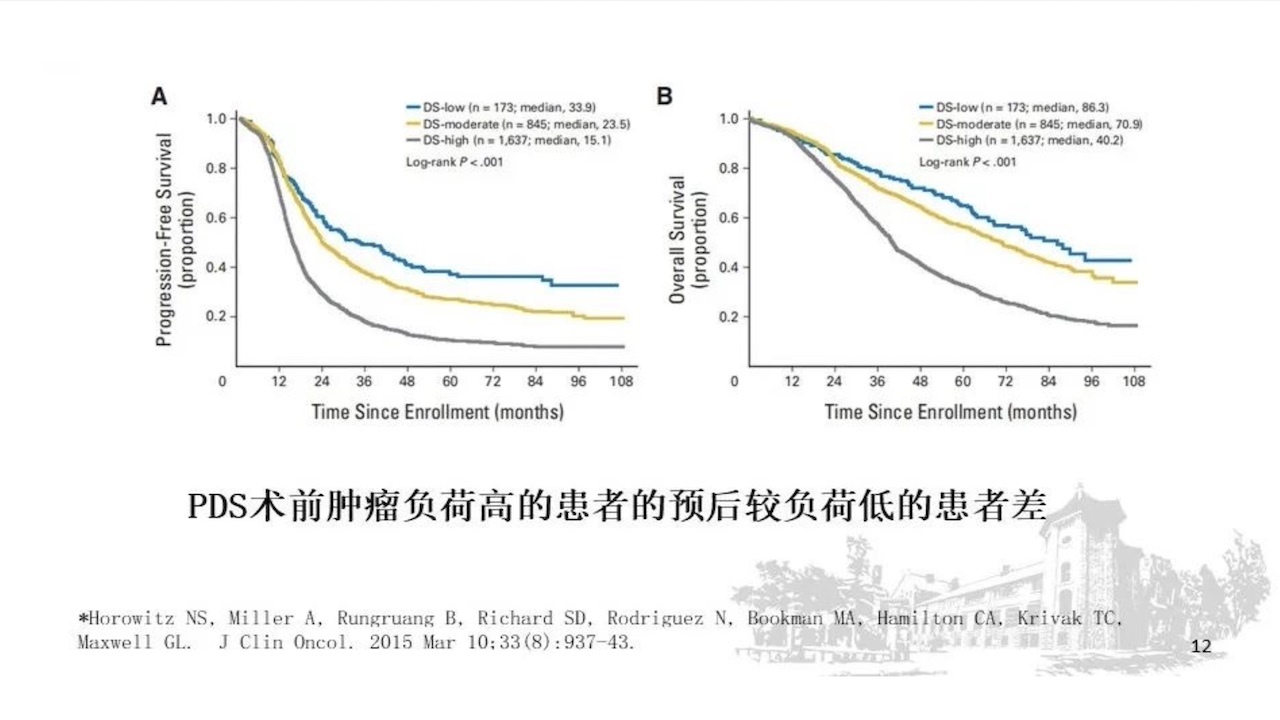
PDS术前肿瘤负荷高的患者的预后较负荷低的患者差,这可能有两个因素,一个是患者没达到R0,另一个是要到达R0,需要进行更为扩大的手术,手术后,术后并发症的升高可能会影响后续治疗,从而抵消手术的益处。
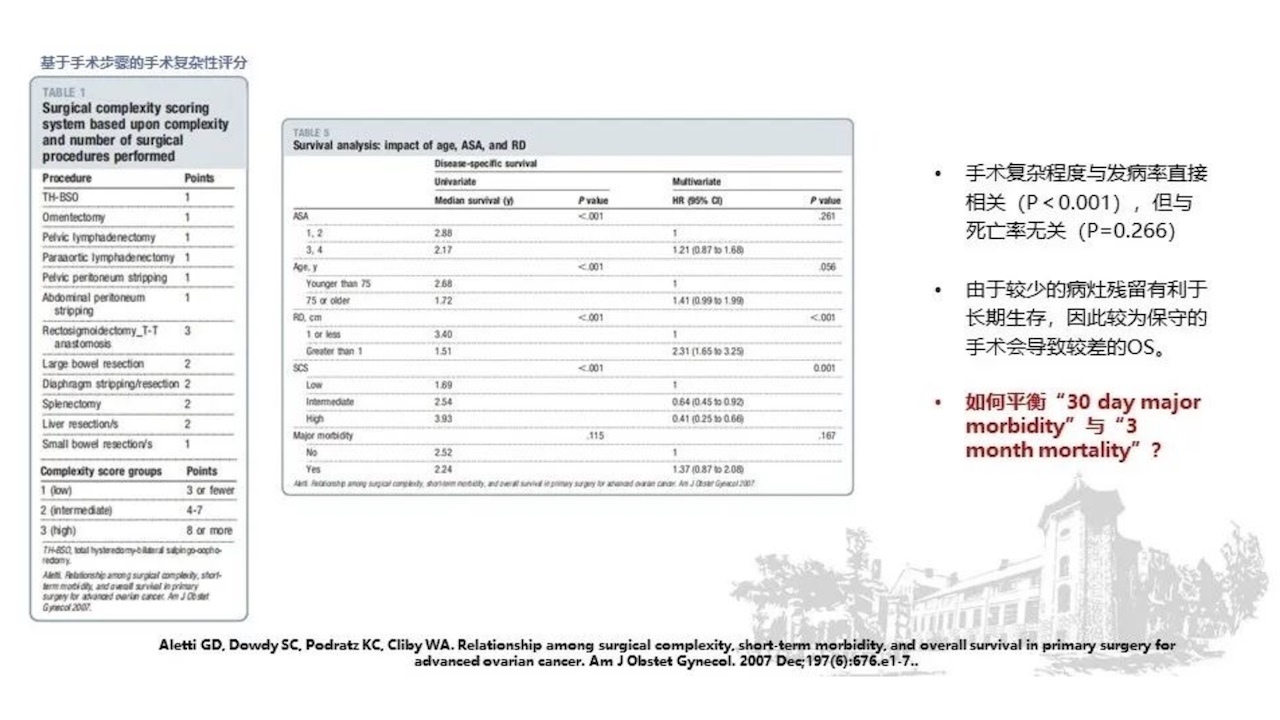
手术复杂程度与高发病率直接相关(P<0.001=但与死亡率无关(P=0.266)。由于较少的病灶残留有利于长期生存,因此较为保守的手术会导致较差的OS。
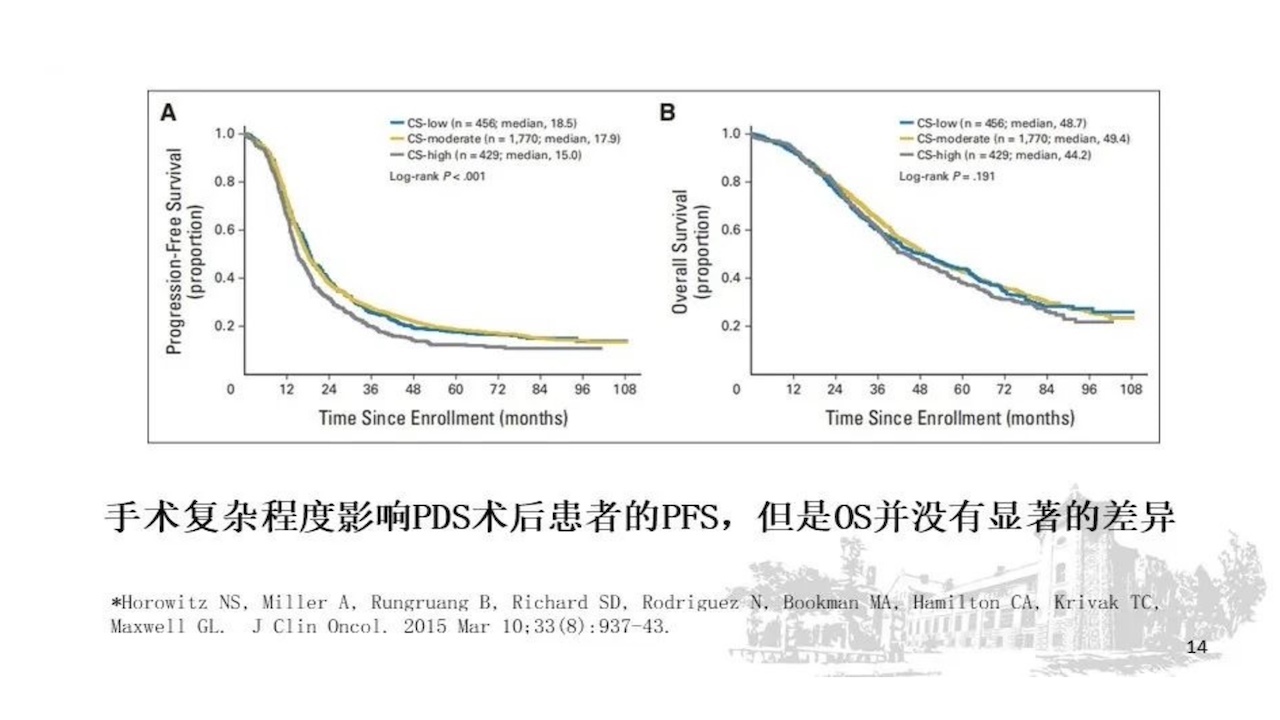
如何平衡患者生存与并发症之间的关系呢?手术复杂程度影响PDS术后患者的PFS,但是OS没有显著的差异。
浙江大学妇产医院大学团队所做的研究,结果发现,只有在肿瘤低负荷患者中R0与长期生存有关;而在肿瘤高负荷患者中R0与长期生存并不相关。
提示:在肿瘤高负荷的晚期高级别浆液性卵巢癌患者中,通过复杂手术而实现R0可能并不能改变患者预后的结局,对于肿瘤高负荷患者不能盲目追求R0。在临床上也体会到,对于上腹部及盆腔的手术,很容易达到R0,对于中腹部肠系膜大的病灶、引起肠系膜挛缩的病灶往往束手无策,往往很难达到R0。应重视生存获益与复杂手术带来的危害之间的平衡,不能过度追求手术的切净而忽视患者的长期生存获益。
微创
随着腔镜手术的开展,腹腔镜在卵巢癌的治疗中也开始应用,但我们不能把腔镜完全等同于微创,微创是一种理念。特别是在早期的卵巢癌手术过程中尽量完整切除肿瘤,避免肿瘤的破裂。腔镜手术在早期卵巢癌中的应用一是再分期手术,或是子宫+双附件切除时意外发现的早期卵巢癌,能完整地切除肿瘤,而且能避免肿瘤破裂的情况下取出。另一个是对于晚期卵巢癌腹腔镜进行评估,确定是进行手术还是新辅助化疗。第三是中间型肿瘤细胞减灭术的应用,也有一些晚期的卵巢癌手术采用腹腔镜手术,到底对患者有无益处,值得我们思考。
NACT+IDS
对于卵巢癌的手术,理想的是初始肿瘤细胞减灭术达到R0,但是有时由于技术因素或患者的因素难以达到,这种情况下可选择新辅助化疗,再选择IDS。新辅助化疗的益处是在保证相似预后的基础上提高达到满意细胞减瘤术的比例,减少围手术期并发症及死亡率。多项的大型的多中心研究显示:晚期卵巢癌患者的初始选择NACT-IDS的生存获益并不劣于手术治疗,生活质量更好及围手术期并发症更少。

下面是新辅助化疗相关研究结论:
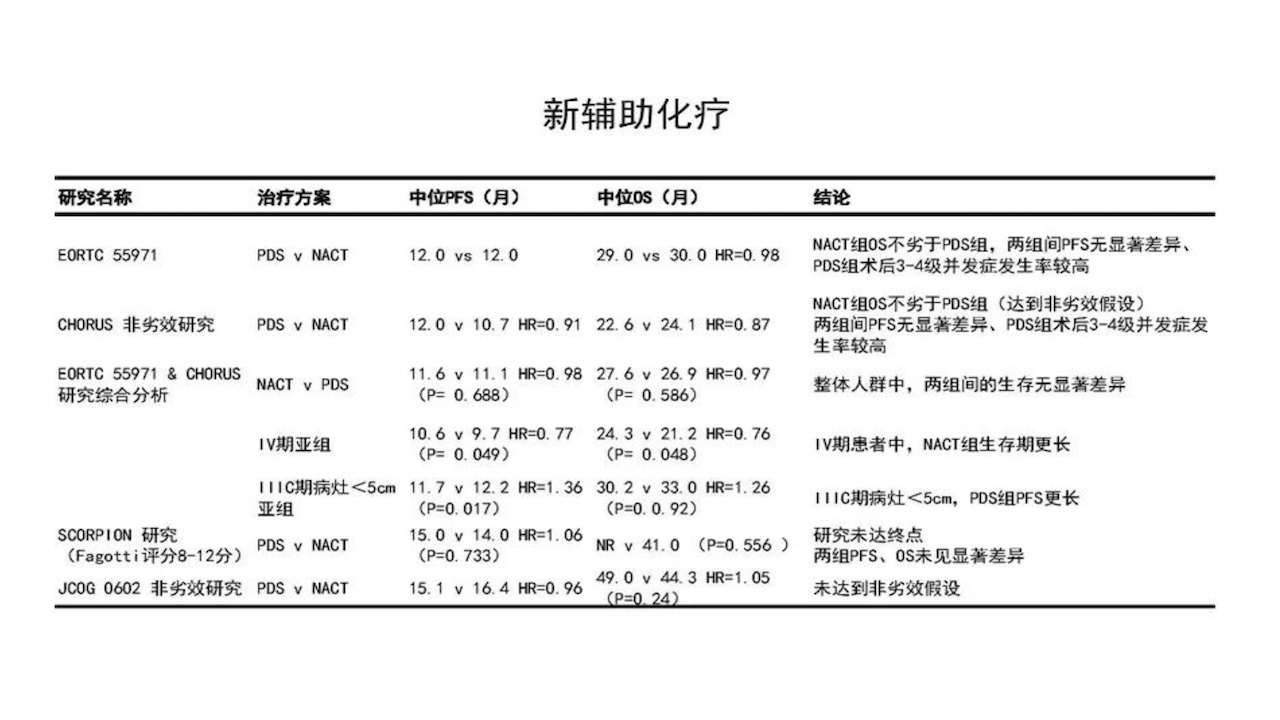
需要强调的是,与PDS相比,NACT+IDS无显著生存优势。
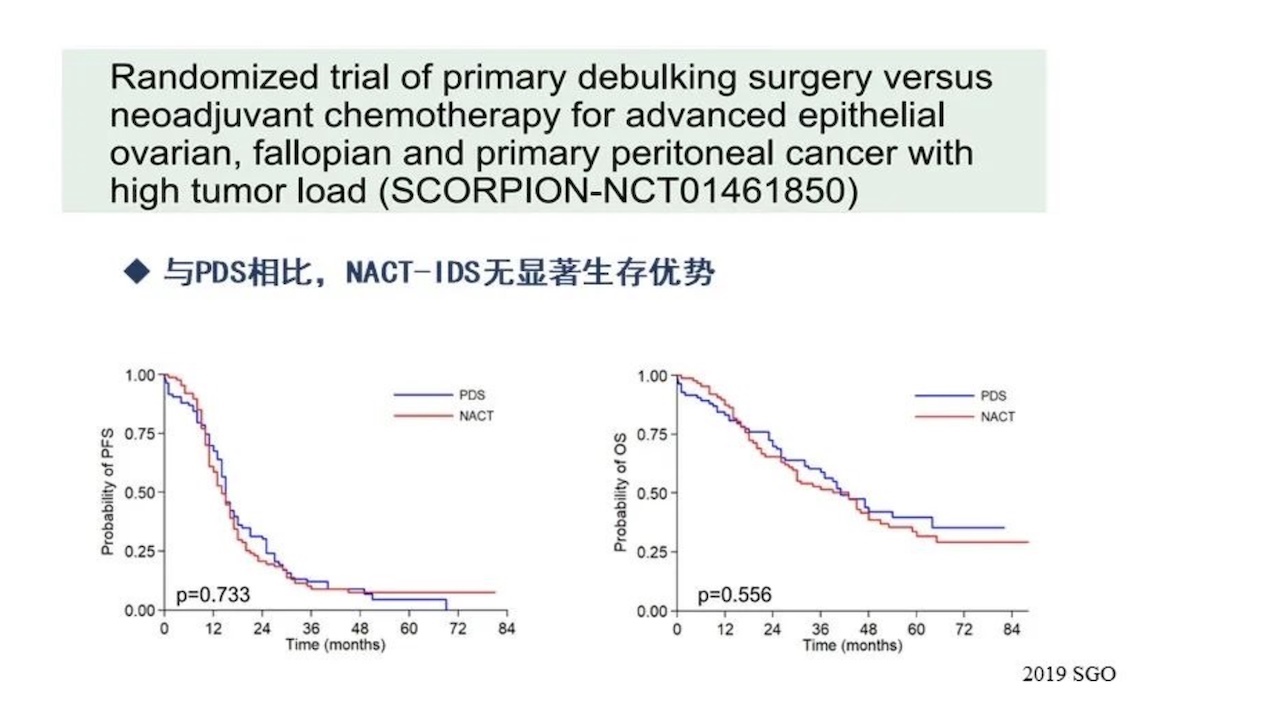
需要注意的是,PDS满意手术不等于NACT满意手术。从残留灶情况对预后影响情况分析可以看出IDS达到的R0的手术相当于初始肿瘤细胞减灭术RI的水平。
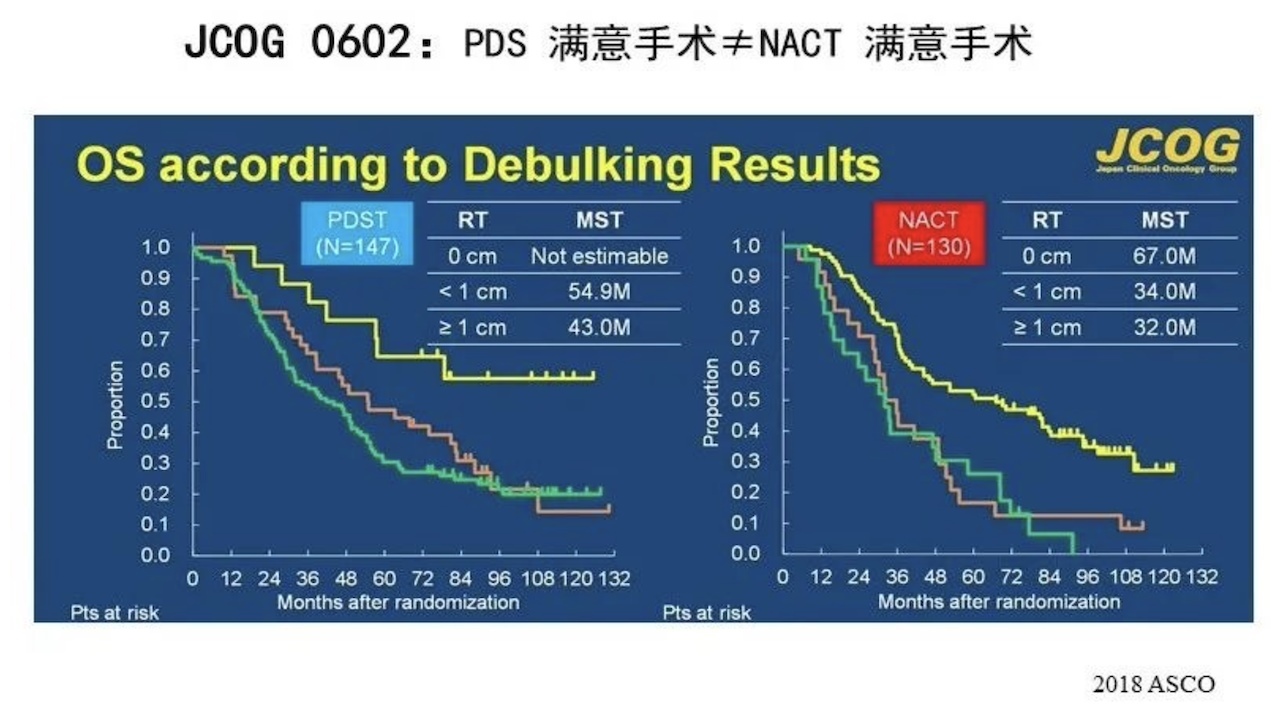
新辅助化疗(NACT)存在的弊端:
并非所有患者均可受益于新辅助化疗。回顾性研究发现,新辅助化疗有可能增加卵巢癌患者铂类耐药性,诱导患者对以后的化疗产生耐药,这种耐药会影响长期生存率。
回顾性分析了425例临床病例利用多元Logistic回归分析,结果表明,对于初次使用铂类药物化疗的患者,NACT-IDS组及PDS组耐药率差异无统计学意义,但当复发患者再次使用铂类药物化疗时,NACT-IDS组的耐药率明显高于PDS组(88.8%vs.55.3%,P<0.001)。
丹麦一项研究分析了自2005年1月至2011年10月1677例AEOC患者的相关数据。结果表明,在PDS组(31.9月)及NACT-IDS组(29.4个月)中位OS差异无统计学意义。NACT-IDS组有着更短的手术时间,手术难度、术中失血量、并发症及术后残瘤的概率均明显降低。但经多变量分析,随着时间的延长,NACT-IDS与2年后的死亡率升高具有相关性,死亡率高达81%。
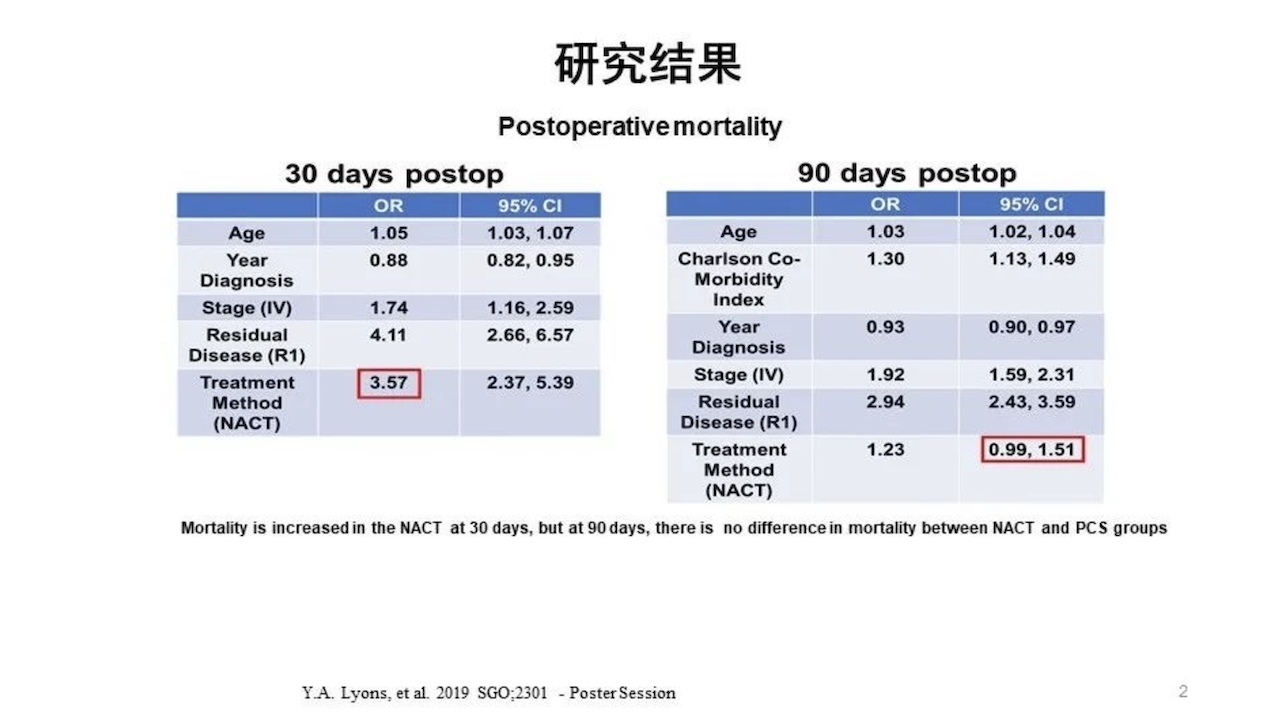
间歇减瘤术不值得等待,基于美国国家癌症数据,比较PCS与NACT/IDS的研究,结果如下所示。
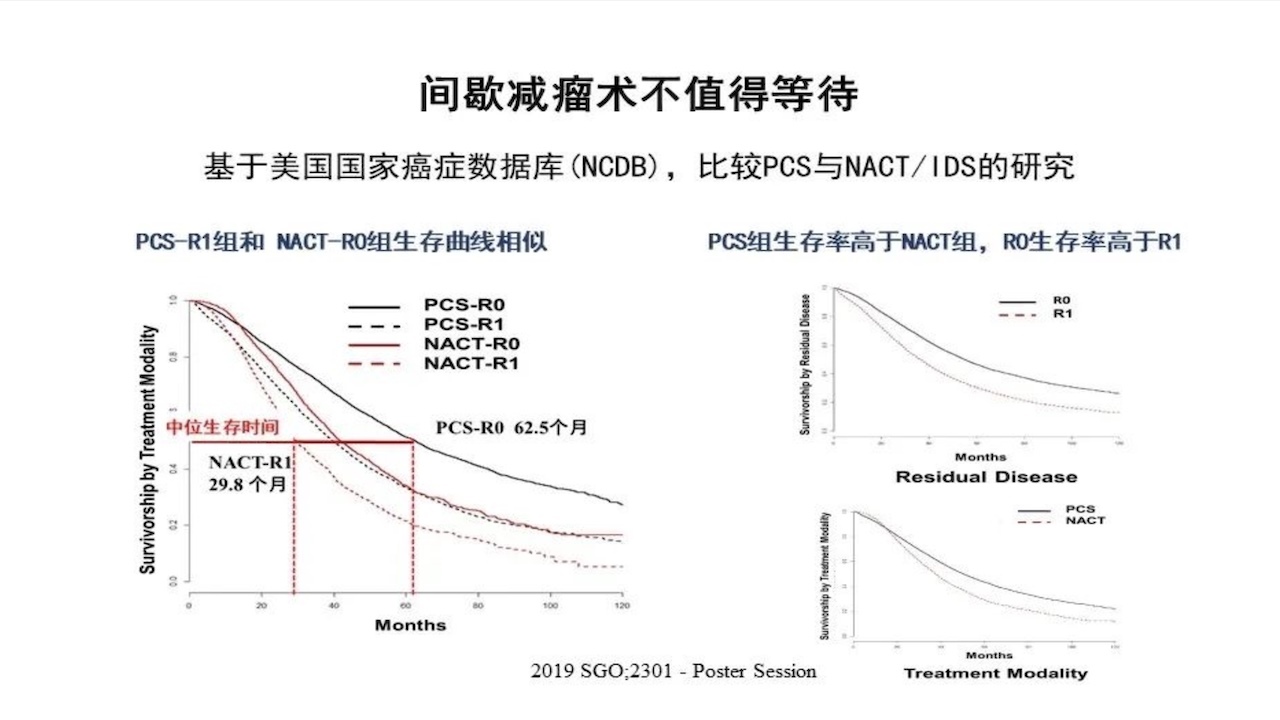
研究结果提示,NACT组术后并发症发生率不仅没有减少反而升高,对于研究结果应该辩证的看待,因为选择NACT的患者本身就是存在合并症或疾病晚期的患者,这些患者本身就存在预后的不利因素或并发症高风险。
对于新诊断的晚期卵巢癌NACT应如何选择?
SGO&ASCO新诊断的晚期卵巢癌的新辅助化疗指导原则(2016):
由妇科医生判断IIIC期货IV期EOC是否能行PDS围手术期风险高或肿瘤细胞减灭术难以实现满意减瘤<1cm*;应行NACT肿瘤细胞件减灭术较大可能实现满意减瘤<1cm*,推荐优先行PDS适合PDS但妇瘤医生认为不可能实现满意减瘤<1cm*,推荐优先行NACT。
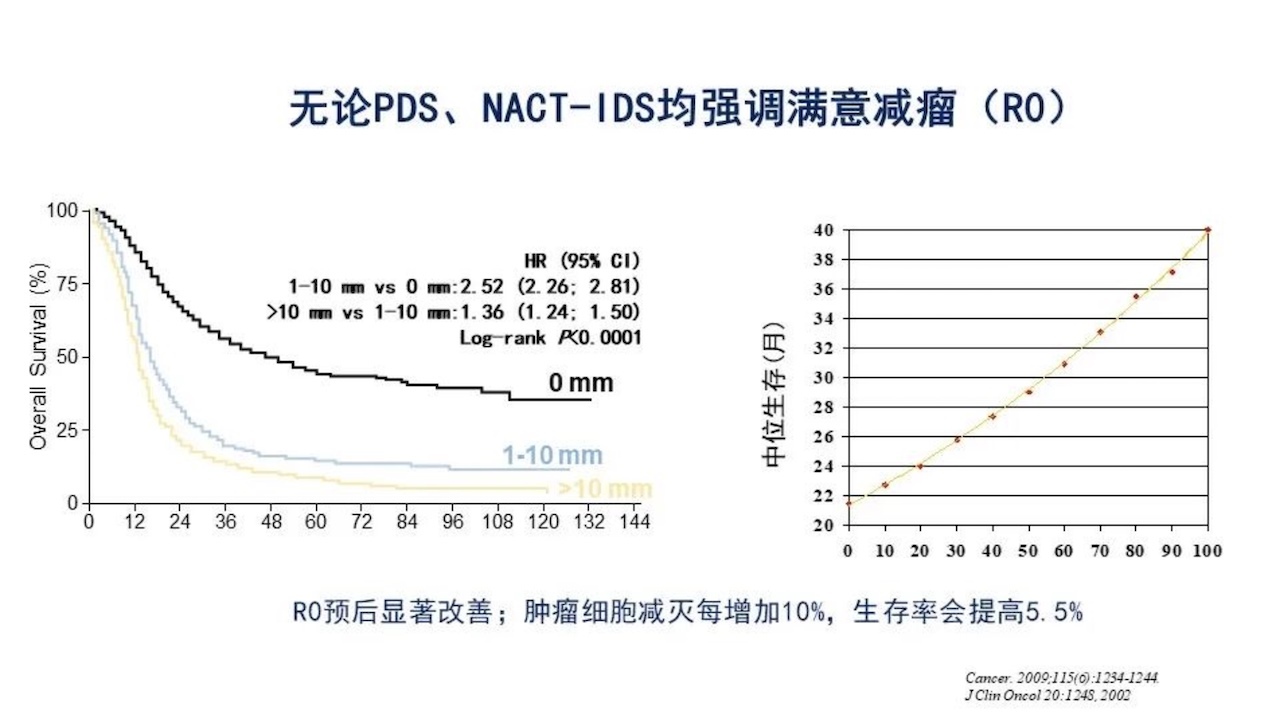
但是无论PDS/NACT+IDS均应强调R0。R0预后显著改善,肿瘤细胞减灭每增加10%,生存率会提高5.5%。
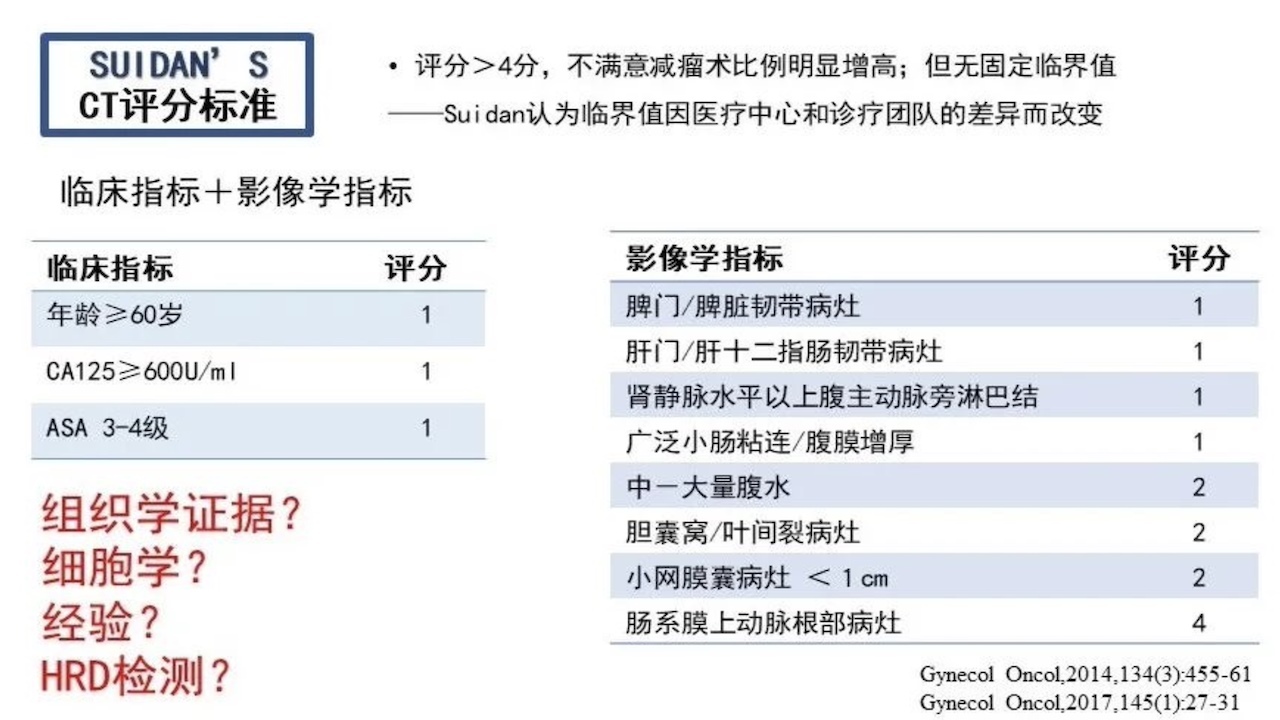
对于晚期卵巢癌患者如何评价能不能达到满意的肿瘤细胞减灭术,要基于团队能力及MDT的支持,此外还要客观的评分,如FAGOTTI评分或SUIDAN’S评分进行。如果患者评估后不能进行满意的R0,可以先进行NACT。化疗前要不要获取组织学证据,细胞学还是医生经验,如果要活的组织学证据,可以进行CT或超声阴道下穿刺来获得组织学证据,对于获得的组织是不是要进行病理检测,根据病理结果初步判断患者预后及处理原则、手术处理原则。
除了FAGOTTI评分和SUIDAN’S评分外,梅奥诊所也提出了自己的评分标准,经过验证后,也有一定的可行性。
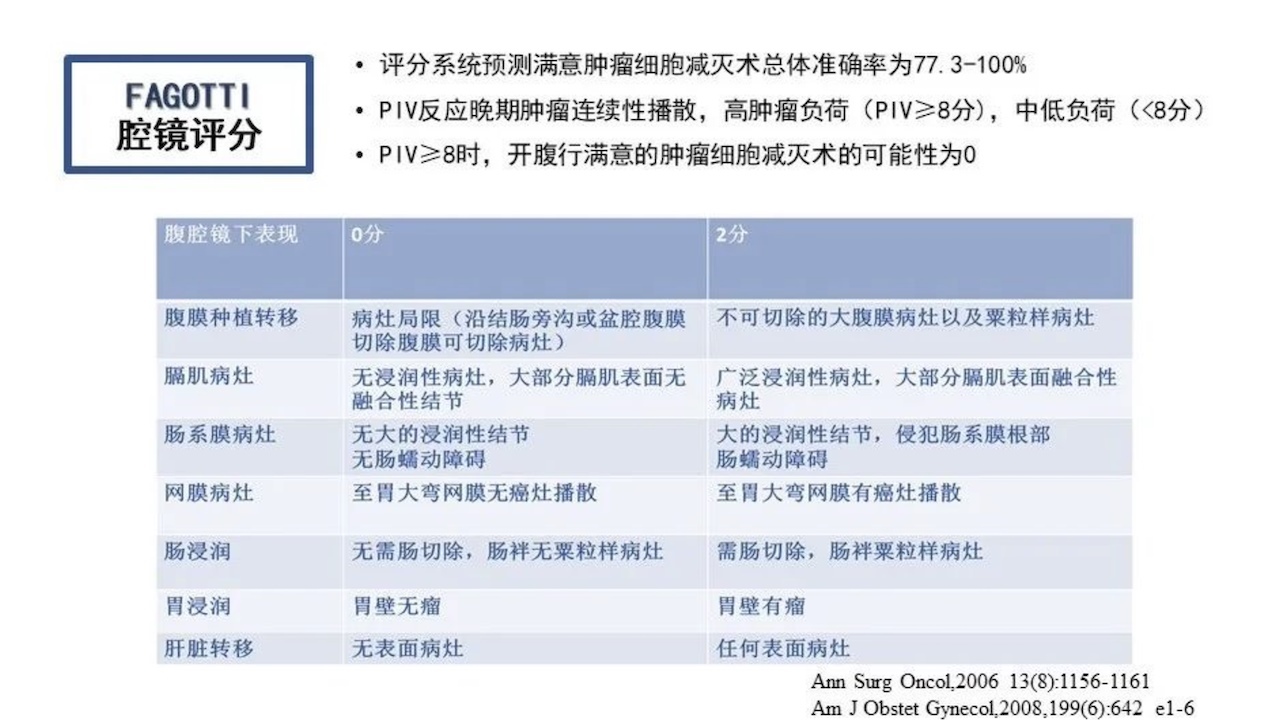
晚期卵巢癌新辅助化疗后采用间歇性减瘤术,除了开腹手术也可以进行腔镜手术。
淋巴结切除术
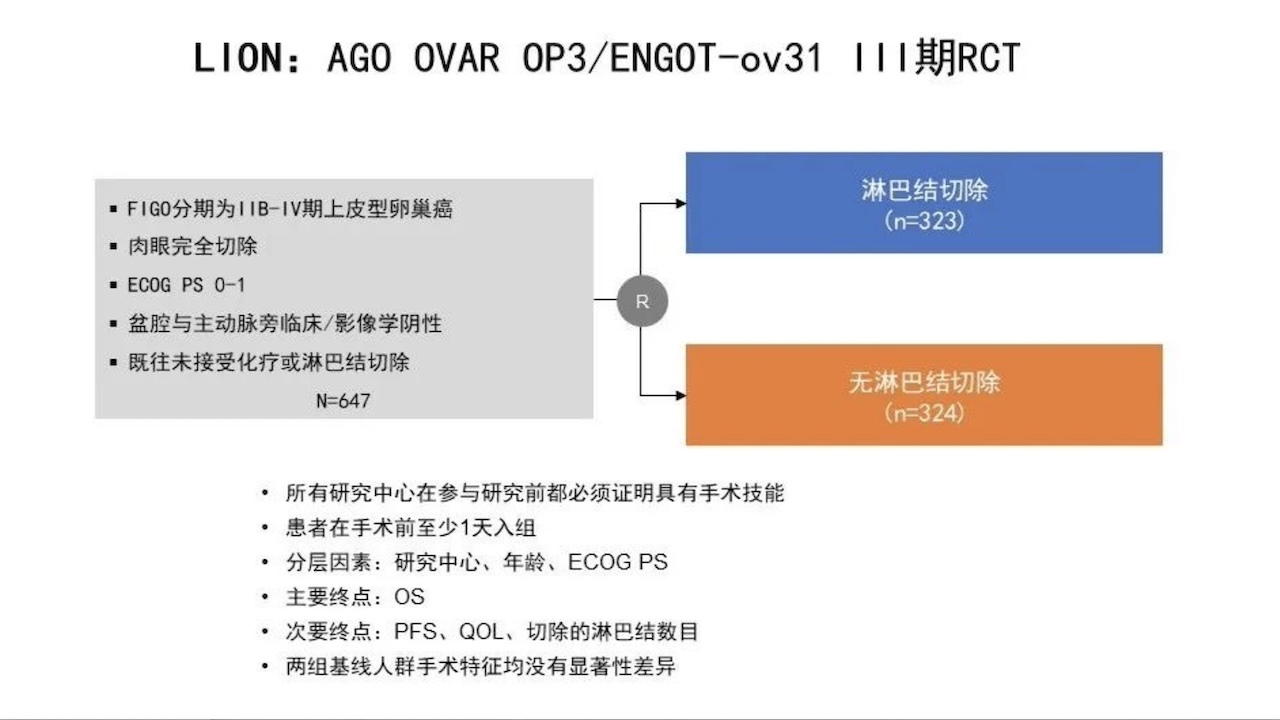
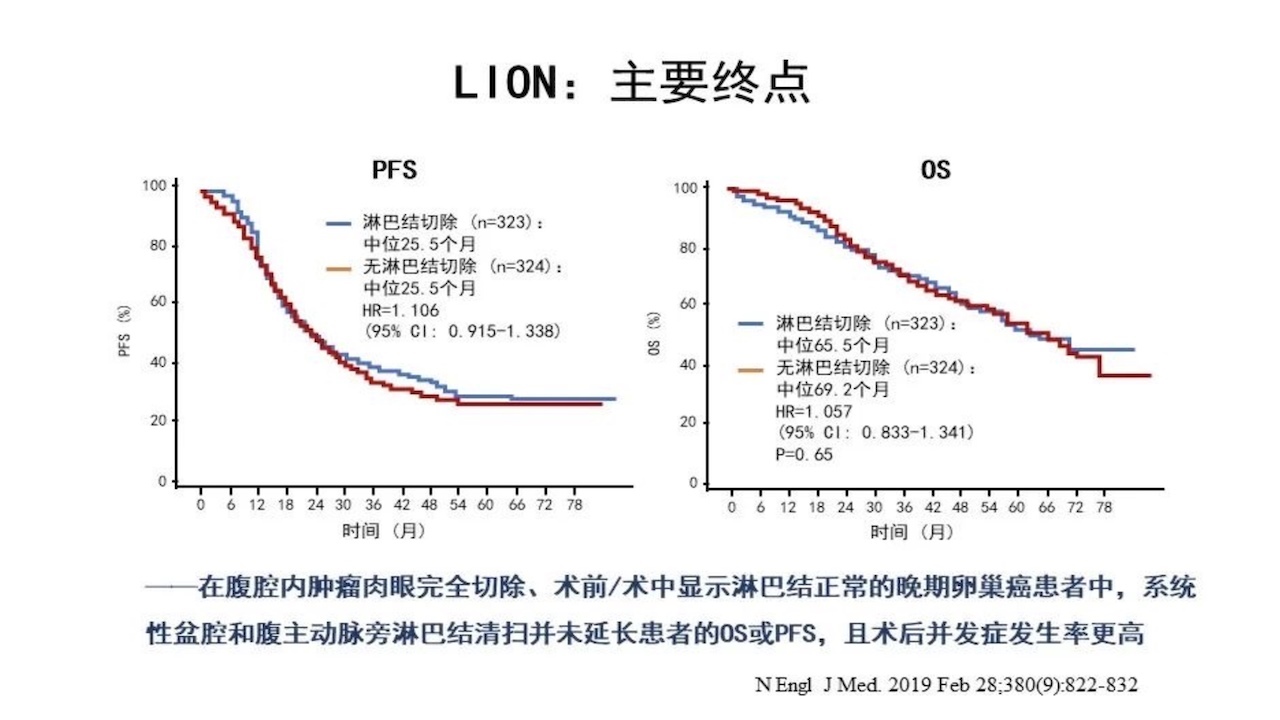
对于恶性肿瘤的手术,淋巴结切除术是重要的组成部分,对于晚期卵巢癌的手术,淋巴结是不是一定要切除,让我们来看一下LION研究的结论。
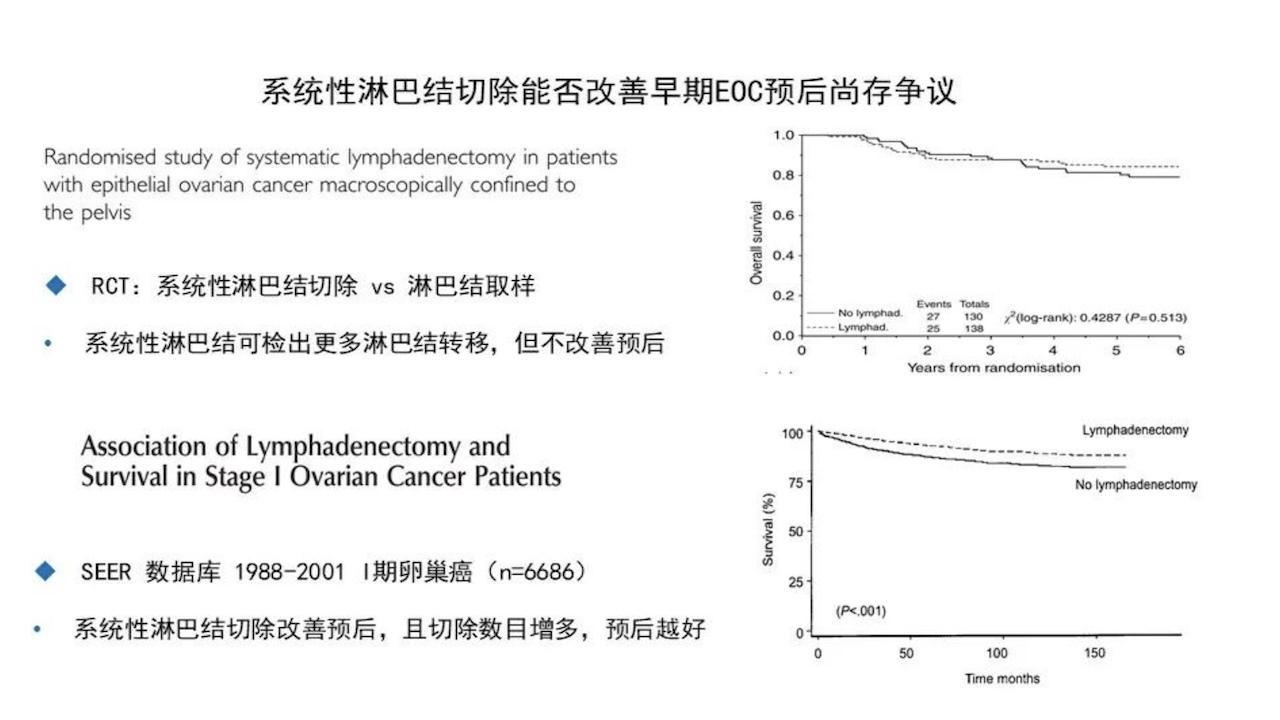
对于早期EOC,系统性淋巴结切除能否改善患者预后尚有争议
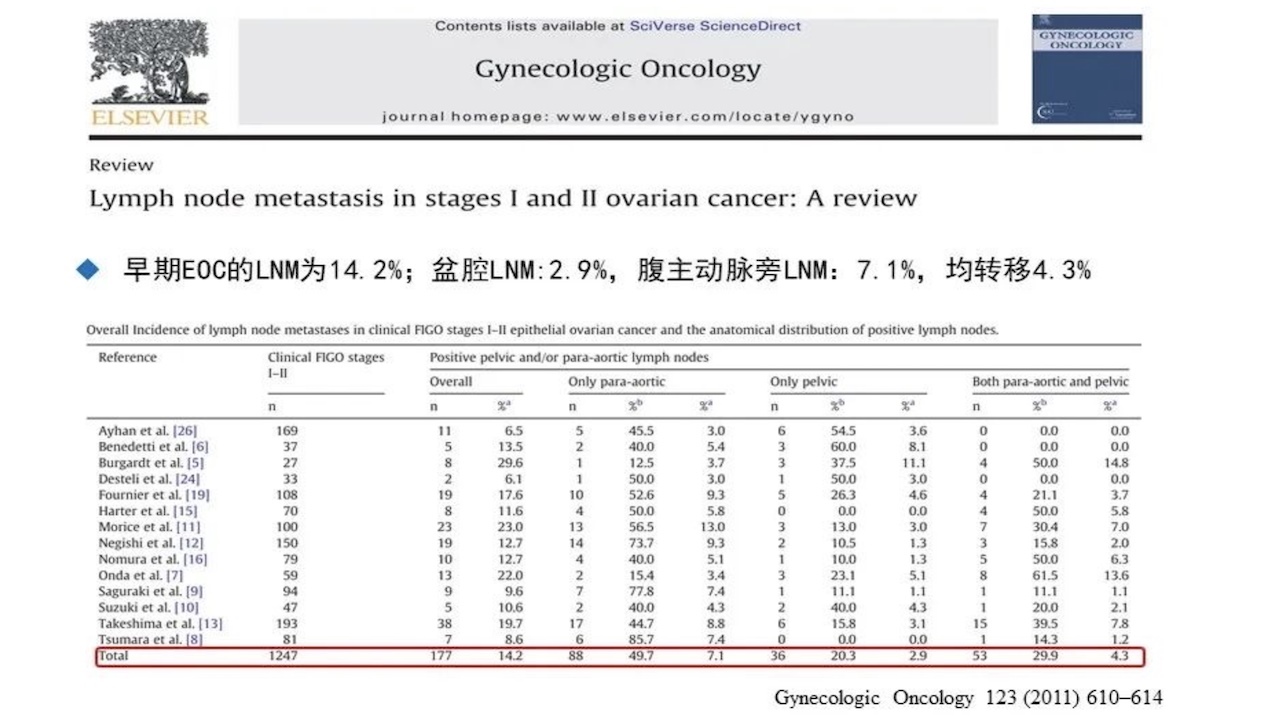
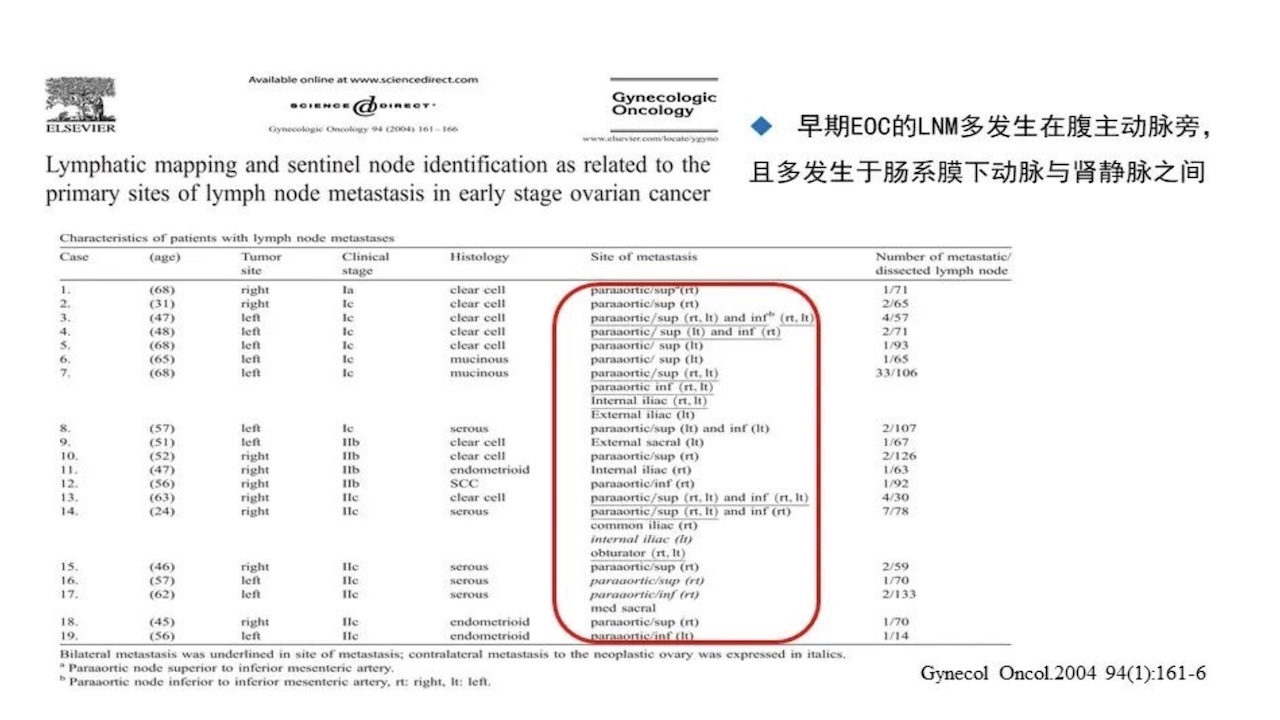
早期卵巢癌的LNM为14.2%,盆腔LNM为2.9%,腹主动脉旁LNM为7.1%,均转移4.3%。
早期EOC的LNM多发生在腹主动脉旁,且多发生于肠系膜下动脉与肾静脉之间,我们在临床上做腹主动脉旁淋巴结的清扫往往做到肠系膜下动脉的水平,有可能把大多数转移的淋巴结遗漏掉,手术达不到预期效果,这种手术还有没有必要,值得思考。
对于淋巴结的切除有以下共识:
卵巢癌肿瘤位于盆腔:
*切除下腔和腹主动脉旁两侧淋巴结,至少肠系膜下动脉、最好肾静脉水平
*双侧盆腔淋巴结各组淋巴结
累及盆腔及上腹部:
*切除能切除或肿大淋巴结;临床阴性的淋巴结不需切除(2019V1NCCN指南新增特征)
*盆腔外肿瘤病灶≤2cm者(即IIIB期),应行双侧盆腔和主动脉旁淋巴结切除术(2021.v1删除此条)
临床上还有另一种情况,如果没有进行彻底全面分期手术,术后存在高危因素,确定要进行化疗,对这部分患者是进行再分期包括淋巴结的切除还是不再手术直接进行化疗,通过研究显示,对于淋巴结小的转移可以通过术后化疗来控制。对于早期的高危患者,术后一定要进行化疗或者早期没有进行完全分期的患者,术后病理提示存在高危因素需要化疗的患者,要不要再进行淋巴结的切除值得我们思考。对于低危患者为了分期进行淋巴结切除有没有必要同样值得我们思索。
对于铂敏感复发的患者,完成术后化疗6-12个月以上复发的卵巢癌患者若为孤立病灶(或局限性)适合完全减灭并且没有腹水的患者,可考虑SCS。
这只是一个总体的指导原则,实际上有多个评估模型来帮助我们筛选适合手术的患者。


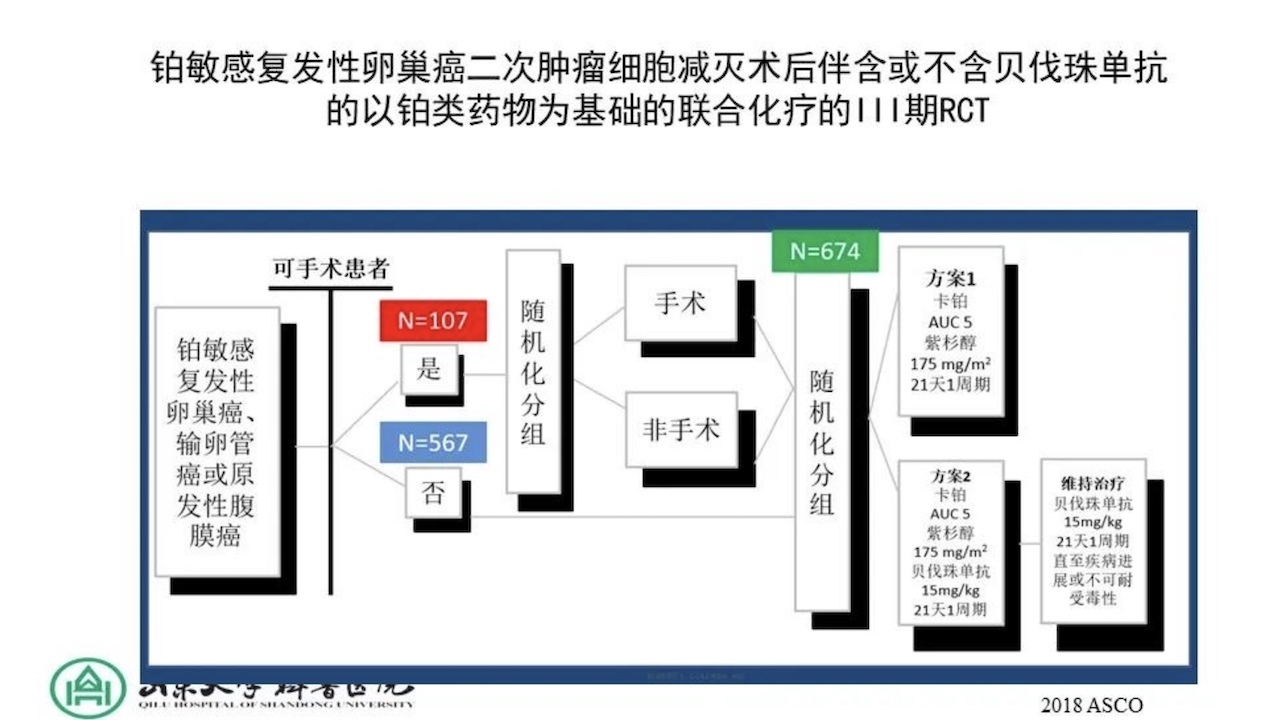
铂敏感复发性卵巢癌二次肿瘤细胞减灭术后伴含或不含贝伐珠单抗的以铂类药物为基础的联合化疗的III期RCT。结果显示
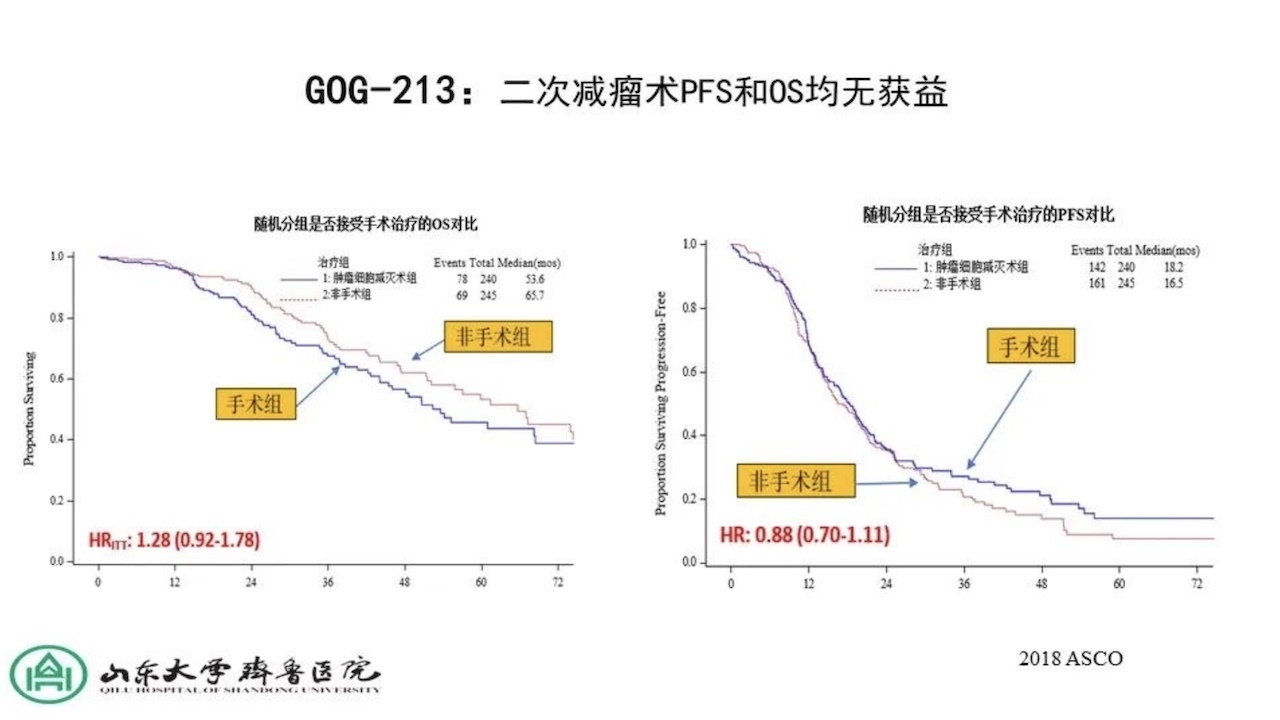
亚组分析:
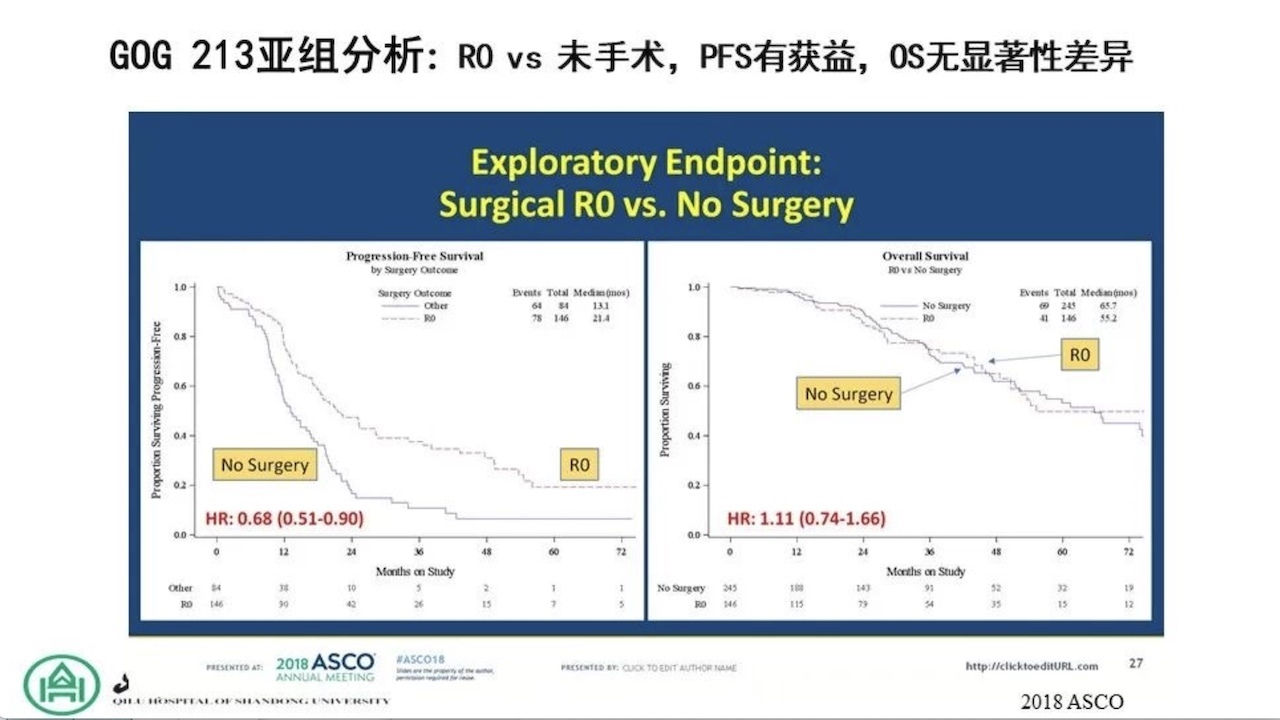
手术没有完全切除的患者比未手术患者疗效差。
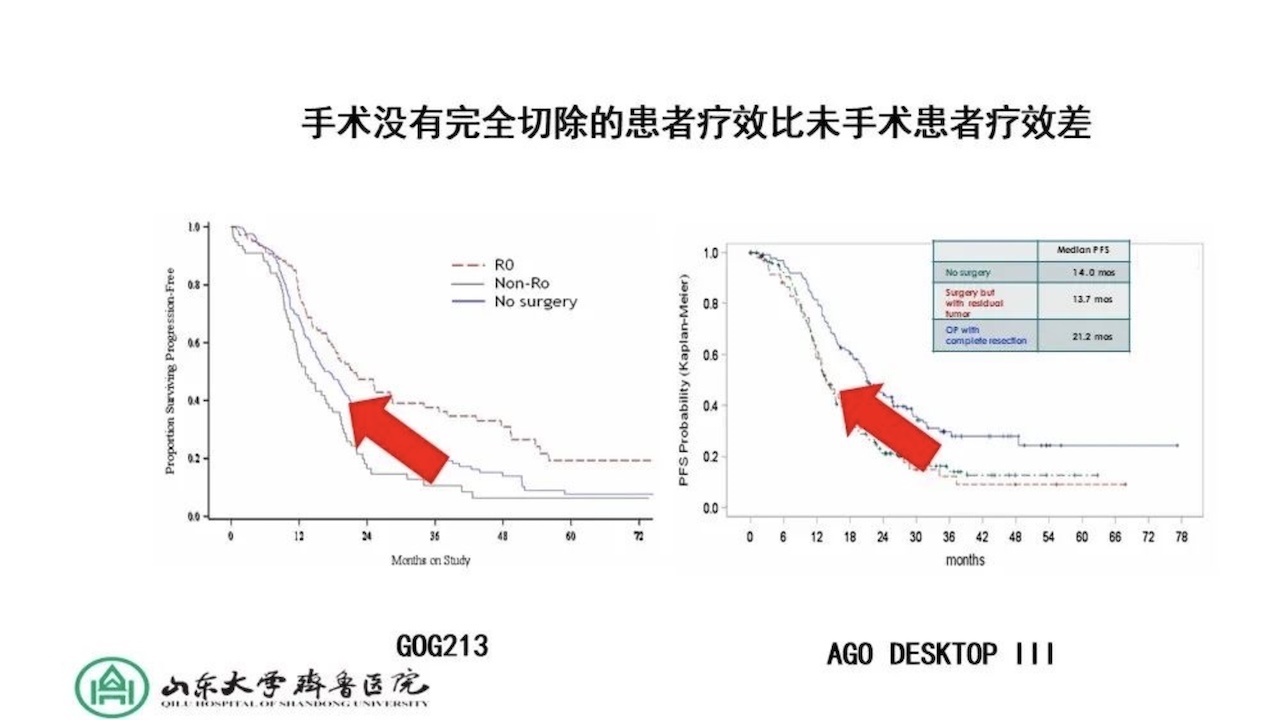
另一个研究,二次肿瘤细胞减灭术在复发性卵巢癌治疗中作用的RCT,AGODESKTOPIII/ENGOTov20的中期分析,结果显示手术组vs非手术组:中位PFS都显著获益。
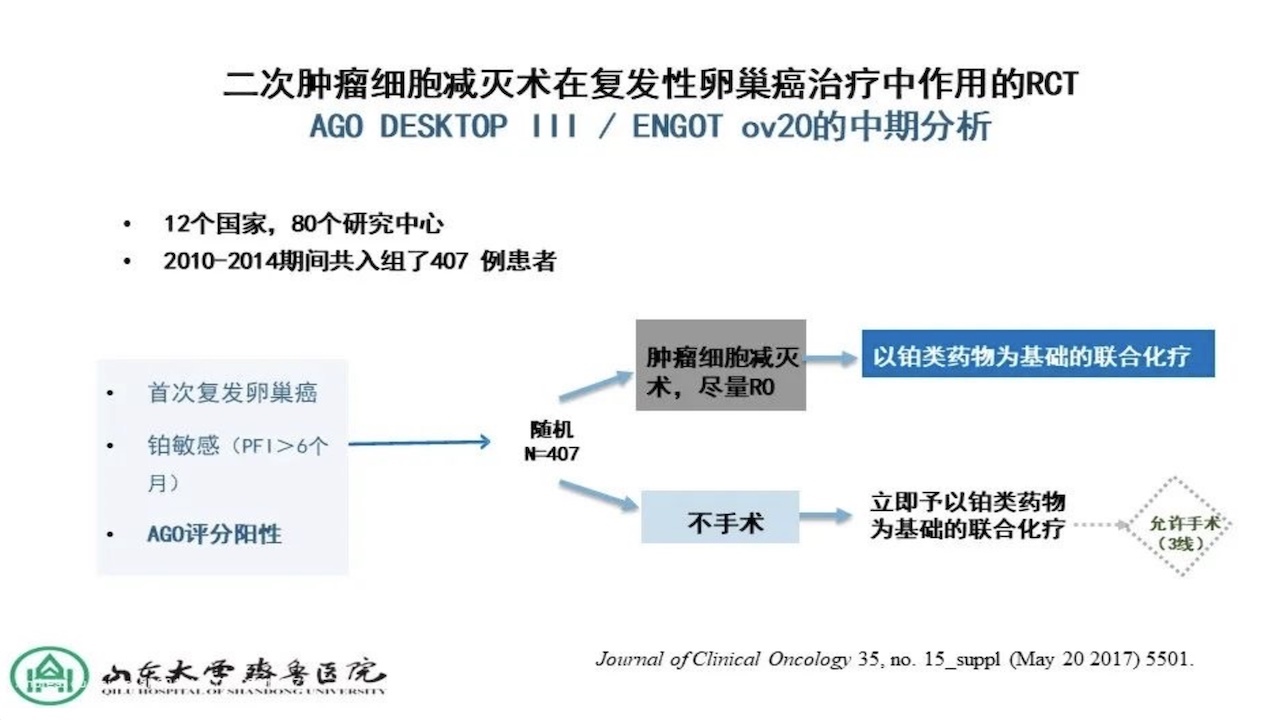
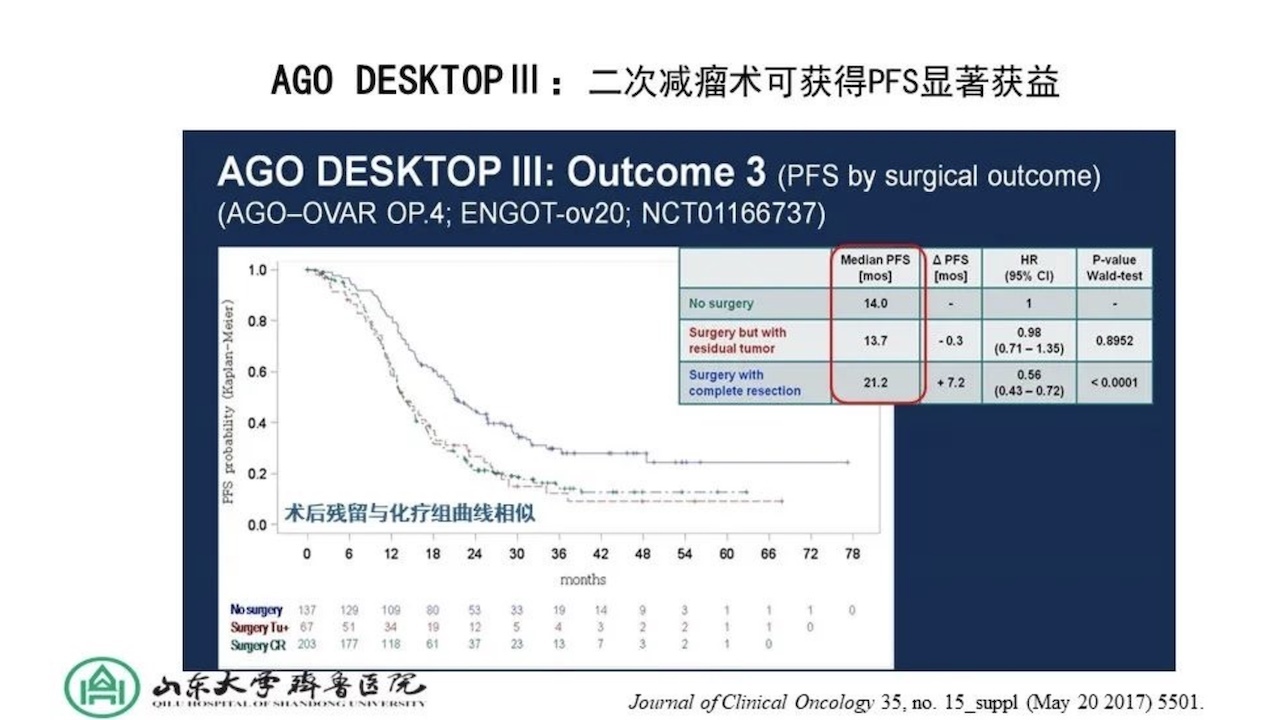
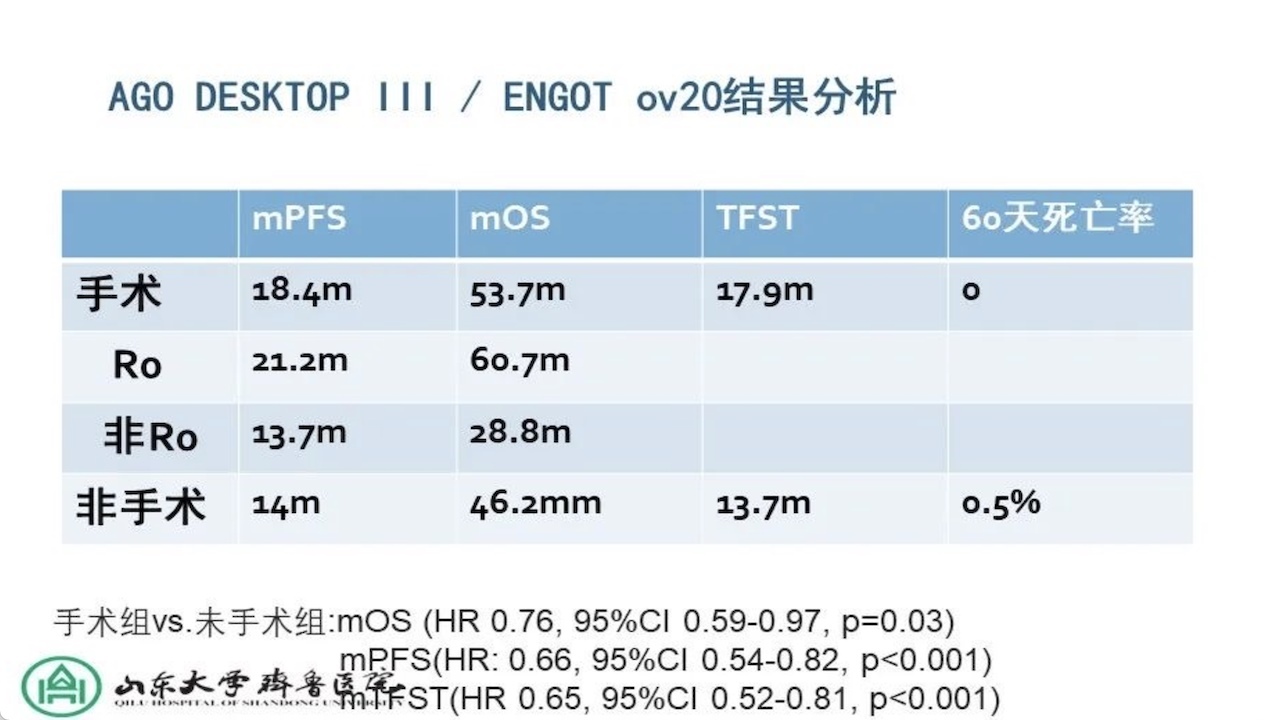
DESKTOPIII与GOG2013研究设计对比如下。
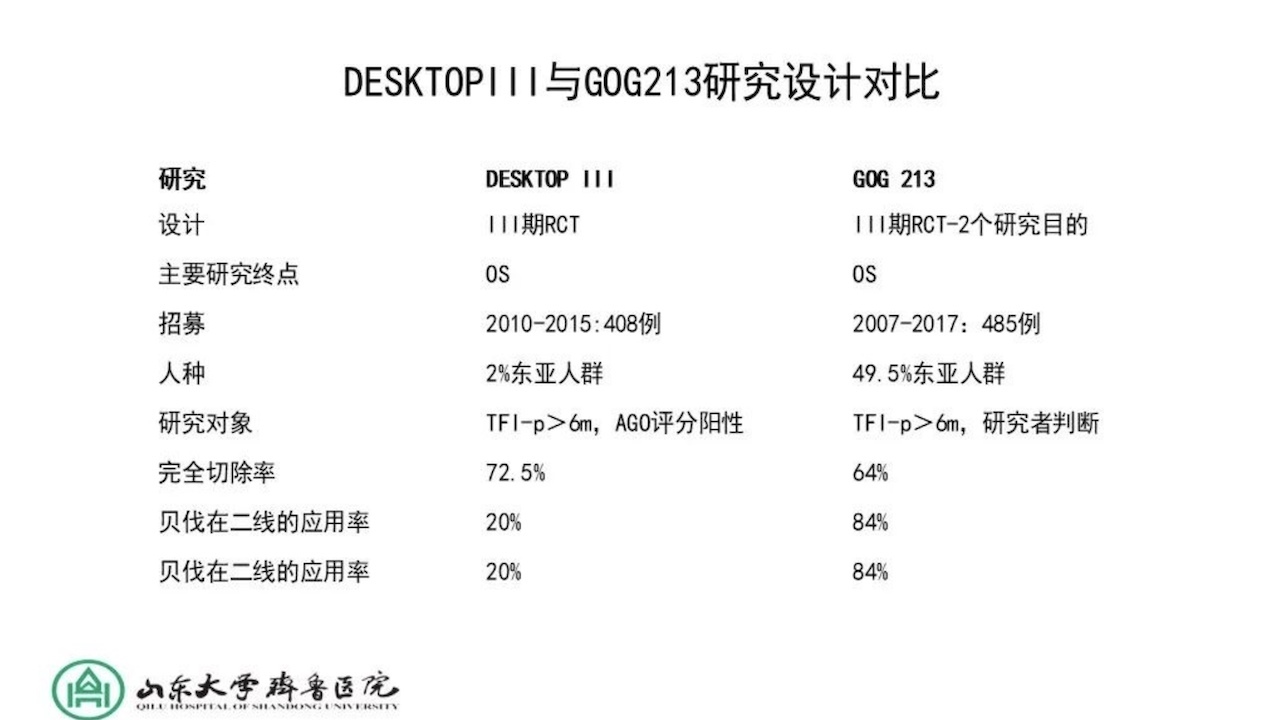
两项研究取得不同结果,有多种可能,包括入组患者的差异等等,但比较可以看到两者贝伐单抗的应用存在差异,铂敏感复发患者加用贝伐单会不会抵消手术的获益值得关注与研究。
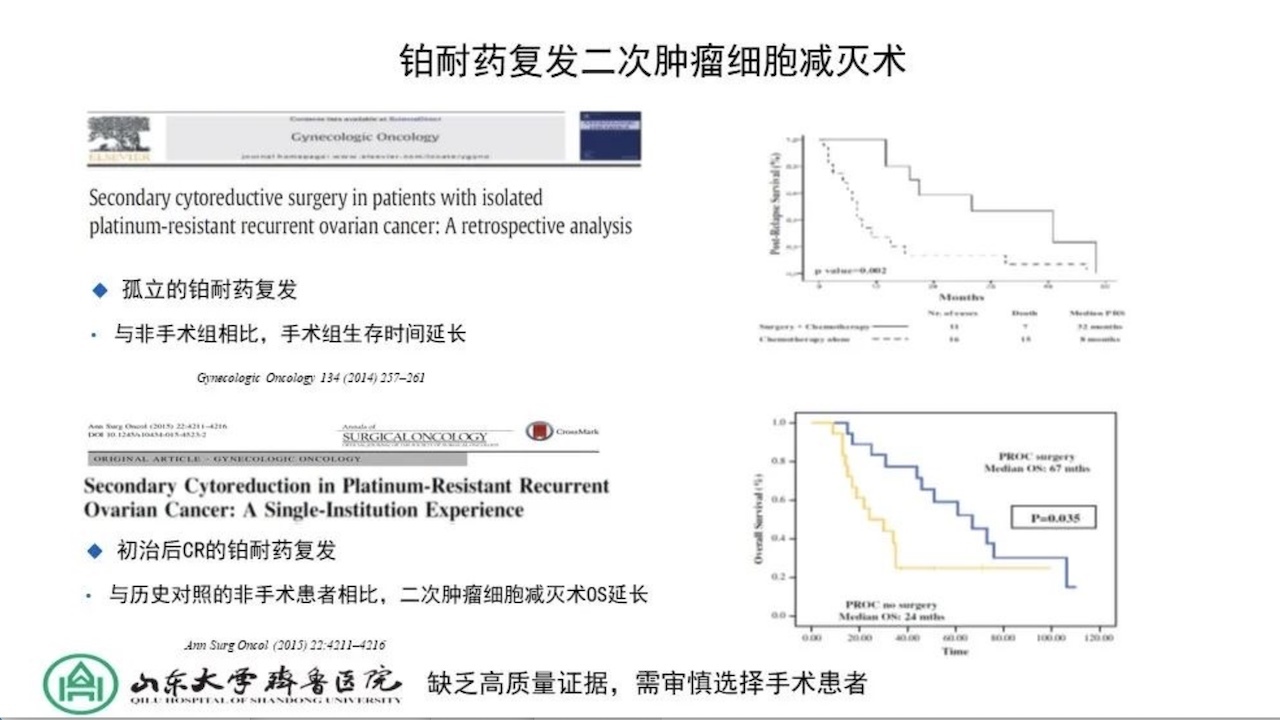
铂耐药复发二次肿瘤细胞减灭术到底是否可行,早期的研究是对孤立的铂耐药复发与非手术组相比,手术组生存时间延长。但是是孤立的病灶。对于初始后CR的铂耐药复发,与历史对照的非手术患者相比,二次肿瘤细胞减灭术OS延长。但是都缺乏高质量的证据。
总之,在卵巢癌的治疗中,手术治疗是基础,合理地手术需要我们有更多的探索和思考。
[声明:本网站所有内容,凡未注明来源为“转载”,版权均归巢内网所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:巢内网”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们]



