
步态障碍是帕金森病运动功能受损的典型症状。尤其在病情发展到中晚期时,患者起步、行走和转身等动作会变得更为艰难,常表现出慌张步态、冻结步态以及姿势平衡失调等问题,而这些情况正是引发帕金森病患者跌倒甚至致残的关键因素。本文结合最新临床研究证据及专家共识,对帕金森病步态障碍的评估方法及治疗策略进行系统梳理,为临床诊疗及患者管理提供参考。
一、临床评估
1、评估流程
帕金森病步态障碍的评估流程包括病史采集、临床观察、临床测试、量化评估、评估档案。最终完善患者步态、姿势与平衡(含冻结步态)的评估(见图1)。
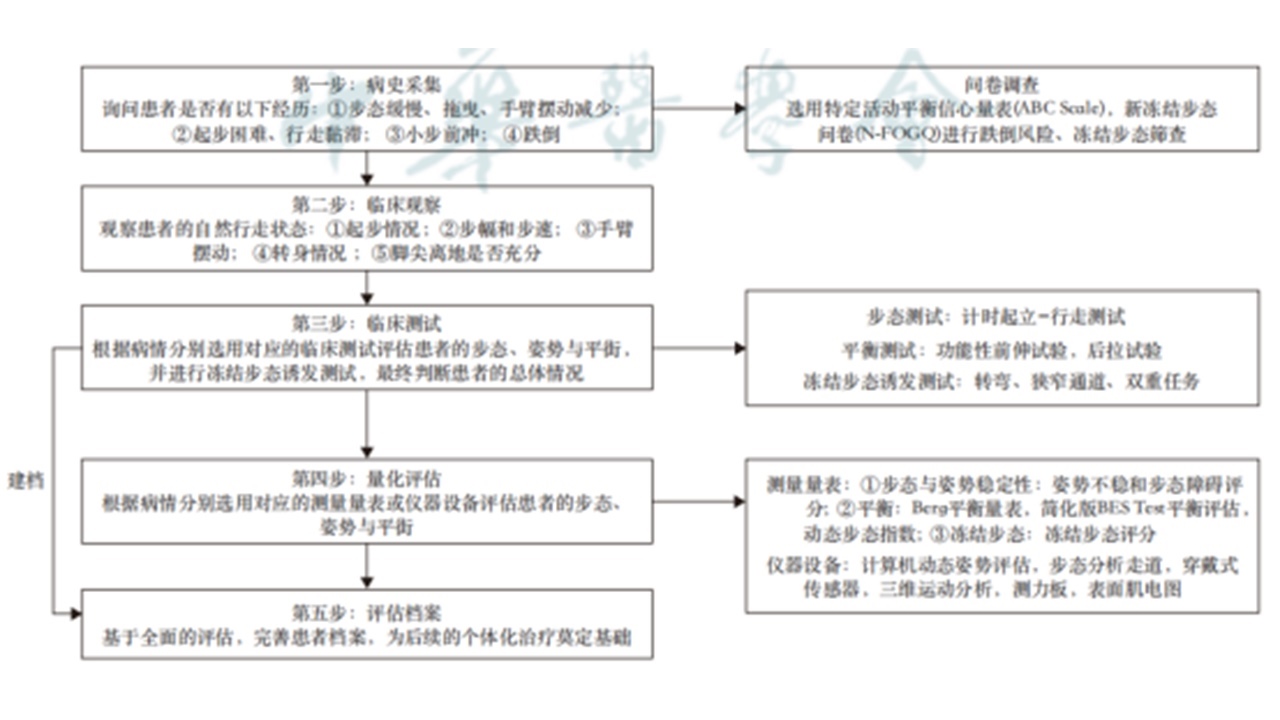
图1
2、评估方法
(1)问卷调查:新冻结步态问卷(N-FOGQ)专门评估冻结步态的严重程度,通常得分越高症状越重;特定活动平衡信心量表(ABCScale)主要用于评估患者对自身平衡功能的信心,得分越低,提示平衡功能越差,跌倒风险越高。
(2)测量量表:姿势不稳和步态障碍评分主要是评估步态/平衡困难及识别运动亚型;Berg平衡量表(BBS)属于综合量表,同时反映动态和静态平衡功能;简化版BESTest平衡评估更专注动态平衡评估;动态步态指数(DGI)是动态平衡测试的专门指标;冻结步态评分是专门检测冻结步态及其严重程度。
(3)临床测试:计时起立-行走测试(TUG)是最常用的步态测量工具,但不适用于使用助行器的患者;功能性前伸测试(FRT)主要用于快速简便确定身体稳定性;后拉试验主要用于评估姿势稳定性;冻结步态诱发试验主要包括转弯、狭窄通道、双重任务等,用于诱发和评估冻结步态。
(4)仪器设备:计算机动态姿势评估包含感觉整合、平衡极限、运动控制测试;步态分析走道主要是步道上的力传感器测量步态时空参数;穿戴式传感器主要是传感器(加速度计、陀螺仪)测量步态时空参数;三维运动分析系统主要是获取丰富的人体运动和力学相关参数;测力板主要是测量地面反作用力,以计算关节力矩等动力学数据;表面肌电图主要是测量静态或行走过程中肌肉的活动强度。
二、治疗策略
帕金森病步态障碍的治疗通常以改善步态、减少跌倒、提高生活质量为核心,遵循个体化、综合化原则,结合病情制定药物、神经调控、物理治疗及代偿策略的多维度方案。治疗流程见图2。
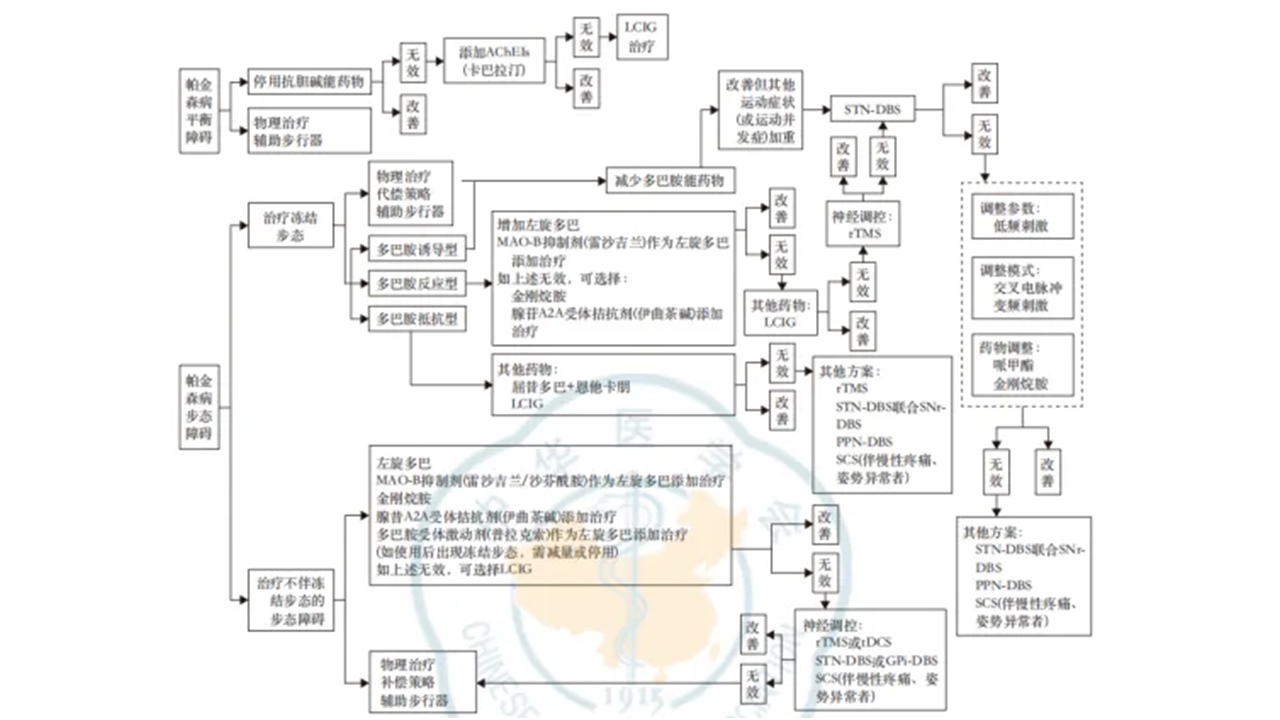
图2
(一)药物治疗
1、左旋多巴及左旋多巴/卡比多巴肠凝胶(LCIG)
左旋多巴是治疗帕金森病的核心药物,也是改善帕金森病步态障碍(包括冻结步态)的一线选择,尤其适用于多巴胺反应型冻结步态。
临床研究显示,其可缩短患者“关”期,降低冻结步态发作频率,但部分患者改善冻结步态的剂量阈值更高,需在不加重异动症的前提下适当调整剂量。
此外,与标准的口服左旋多巴治疗相比,连续空肠内持续灌注LCIG可维持血浆左旋多巴水平的稳定,尤其适合中晚期患者,并且对多巴胺抵抗型冻结步态也有一定效果。
2、单胺氧化酶B(MAO-B)抑制剂
通过抑制多巴胺降解提高其水平,改善步态及平衡,常用雷沙吉兰、沙芬酰胺,作为左旋多巴添加治疗,适用于中晚期伴有症状波动的患者。
3、金刚烷胺
金刚烷胺可通过促进多巴胺释放、抑制多巴胺再摄取,改善帕金森病患者的步态及平衡功能,尤其适用于丘脑底核脑深部电刺激(STN-DBS)术后仍有步态障碍的患者,也可用于改善冻结步态。
4、多巴胺受体激动剂
多巴胺受体激动剂可直接刺激多巴胺受体,改善帕金森病患者的步态障碍,常用药物包括罗替戈汀(透皮贴剂)、普拉克索等,可作为单药治疗或左旋多巴的添加治疗。
5、胆碱酯酶抑制剂
卡巴拉汀是常用药物,两项RCT研究发现,卡巴拉汀可减少帕金森病患者的跌倒发生,改善步态稳定性;此外,停用抗胆碱能药物12个月可显著改善冻结步态症状,减少跌倒次数。
6、其他药物
哌甲酯适用于接受了最佳剂量的多巴胺能药物和STN-DBS治疗,但仍有严重步态障碍和冻结步态的患者。
屈昔多巴需与恩他卡朋联合使用,作为左旋多巴的添加治疗,可改善多巴胺抵抗型冻结步态,单独使用屈昔多巴对冻结步态无效。
腺苷A2A受体拮抗剂,如伊曲茶碱作为左旋多巴添加治疗,可改善伴有症状波动患者的步态及冻结步态。
(二)侵入性神经调控
1、脑深部电刺激(DBS)
刺激靶点:包括丘脑底核(STN)、苍白球内侧部(GPi)、脚桥核(PPN)及黑质网状部(SNr)等。在最优左旋多巴服药方案时仍伴有运动并发症的帕金森病患者,可考虑STN-DBS或GPi-DBS,改善帕金森病患者的步态障碍,PPN对帕金森病步态障碍的长期疗效尚不明确;对于药物难治性步态障碍(含冻结步态),可尝试丘脑底核联合SNr刺激改善步态障碍。
STN-DBS的刺激参数及模式:对于高频刺激改善不佳的帕金森病患者,推荐使用低频刺激(60~80Hz)治疗冻结步态,根据患者个体情况调整振幅和脉宽;对于病情复杂的冻结步态,且高频、低频刺激均疗效不佳的患者,建议使用交叉电脉冲刺激或变频刺激,其中变频刺激尤其适用于震颤和冻结步态共存的帕金森病患者。
2、脊髓电刺激(SCS)
SCS最常见的刺激部位是胸段脊髓(78%,其中以T9~T10段最为常见)。SCS具有改善帕金森病步态障碍的潜力,特别是对伴有慢性疼痛、姿势异常的帕金森病患者,可考虑SCS作为辅助治疗选项。
(三)非侵入性神经调控
1、重复经颅磁刺激(rTMS)
rTMS通过快速变化的磁场诱导大脑皮质神经元产生电流,激活特定脑区,从而改善步态障碍及相关症状。其主要刺激靶点包括初级运动皮质(M1)、辅助运动区、背外侧前额叶皮质(DLPFC),其中靶向M1的高频(10Hz)rTMS疗效较为明确。rTMS可作为帕金森病步态障碍(包括冻结步态)的辅助治疗,尤其适用于伴焦虑、抑郁的患者。
2、经颅直流电刺激(tDCS)
tDCS通过电极向特定脑区施加低电流,调节皮质兴奋性,从而改善步态功能。tDCS可作为帕金森病步态障碍的辅助治疗,低成本、便携式、可穿戴tDCS在未来具有辅助家庭治疗的潜力。
3、其他非侵入性神经调控
非侵入性迷走神经刺激(nVNS)初步显示出改善帕金森病患者步态障碍(包括冻结步态)的潜力,可作为探索性的治疗手段。重复经脊髓磁刺激(rTSMS)对帕金森病步态障碍的治疗作用存在争议。
(四)物理治疗
1、感觉提示训练
感觉提示是改善冻结步态最常见的行为疗法,通过外部的时间或空间信息刺激,促进步态的启动和持续,分为视觉、听觉、触觉提示三类。有节奏的运动干预(如舞蹈、音乐或节拍器训练)可更好地改善早、中期患者的步态、步速、步长和平衡。可穿戴提示装置(激光鞋、振动刺激器等)可即刻提高步速,作为辅助训练。
2、步行训练
跑步机训练结合感觉提示和体重支撑,对步长改善效果最佳;减重步行训练可改善患者的运动功能、步长和平衡障碍;机器人辅助步行训练不仅可改善下肢运动功能和平衡,还能有效改善冻结步态。此外,运动-认知双重任务训练(如行走时计数、识物)对步态的改善作用优于单任务训练,可更好地模拟日常行走场景,提高患者的实际行走能力。
3、运动游戏与虚拟现实(VR)康复
运动游戏(包括视频游戏、VR游戏)通过让患者在场景中完成身体运动任务,提高训练的趣味性和依从性,适用于轻、中度帕金森病患者。基于VR的平衡训练,可通过头戴式显示器、传感器等设备,让患者在虚拟场景中进行沉浸式训练,对中晚期患者的平衡功能改善效果优于常规训练。
4、身心运动
常用的包括太极拳、气功、瑜伽等。太极和气功可改善患者的步速、步幅、步行能力和平衡,其中太极的改善效果优于气功,且长期太极训练可延缓帕金森病的疾病进展;瑜伽则可改善早中期患者的平衡受损,作为辅助康复手段。
5、其他物理治疗
有氧耐力训练可作为改善早中期帕金森病步态和平衡的辅助治疗。抗阻训练可辅助改善帕金森病患者的肌力、运动功能、平衡和冻结步态。水中运动可作为早中期帕金森病的辅助治疗策略用于改善姿势平衡。
舞蹈治疗可作为改善帕金森病平衡障碍的辅助治疗。LSVT-BIG可作为改善早中期帕金森病患者平衡和步态的辅助治疗。全身振动训练可改善帕金森病患者的步态。
(五)代偿策略
代偿策略是帕金森病患者步态康复的重要组成部分,通过利用外部刺激、改变运动模式或心理状态等方式,帮助患者改善步态功能,减少冻结步态的发生和跌倒风险。代偿策略需个体化,临床医生应指导患者选择合适方式。
主要分为7类:①利用外部感觉提示;②自我生成刺激;③改变平衡需求;④改变心理状态(如避免焦虑);⑤动作观察与运动想象;⑥采用新步行模式;⑦用其他方式替代行走(如助行器)。
参考文献
中华医学会神经病学分会帕金森病及运动障碍学组,中国医师协会神经内科医师分会帕金森病及运动障碍学组.中国帕金森病步态障碍管理专家共识[J].中华神经科杂志,2025,58(3):228-243.DOI:10.3760/cma.j.cn113694-20240907-00611.
编辑|焦焦
排版|焦焦
审核|三顺
[声明:本网站所有内容,凡未注明来源为“转载”,版权均归巢内网所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:巢内网”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们]

