
卵巢癌是死亡率最高的女性生殖系统恶性肿瘤,中国卵巢癌总体五年总生存(OS)率约为38.9%[1]。SOLO-1研究结果(7年OS率达67%)的公布,证实了利普卓单药维持治疗BRCA突变新诊断晚期卵巢癌的长生存获益,改变了BRCA突变卵巢癌一线维持治疗的格局。然而,在卵巢癌患者中,BRCA突变仅占约25%,而同源重组修复缺陷(HRD)阳性,是合成致死机制的潜在获益人群,检出率可超50%[2],这意味着如果有靶向于HRD的治疗方案,将会令半数以上的卵巢癌患者获益。在此背景下,PAOLA-1研究应运而生,并首次证实了利普卓联合贝伐珠单抗一线维持治疗HRD阳性新诊断晚期卵巢癌可带来具有临床意义的OS改善。
近日,新版国家医保目录公布,利普卓联合贝伐珠单抗一线维持治疗HRD阳性晚期卵巢癌的适应症被新增纳入医保。这意味着,利普卓一线维持治疗卵巢癌实现了的医保全面覆盖,从BRCA突变患者拓宽到更广泛的HRD阳性患者,进一步提升了药物可及性,有望为更多卵巢癌患者带来治愈希望。
虽然多数卵巢癌最初对含铂化疗敏感,但约70%的患者会在3年内复发[1]。患者在经历多次复发后,逐渐会发展为铂耐药,导致预后不良。因此,对于晚期卵巢癌患者,亟需有效延缓复发、延长生存期和增强治愈潜力的一线疗法。
SOLO1研究首次亮相于2018年欧洲肿瘤内科学会(ESMO)大会,结果证实利普卓一线维持治疗可显著改善BRCA突变晚期卵巢癌患者的无进展生存期(PFS),自此拉开了PARPi一线精准维持治疗的序幕[3]。时隔两年之后,2020年ESMO大会公布的SOLO-1研究5年随访数据令人惊艳:利普卓中位PFS长达56个月,较安慰剂组延长了42.2个月,并且48%的患者在5年时未发生疾病进展[4]。
此后,SOLO1研究多次亮相国际舞台,并不断刷新BRCA突变晚期卵巢癌一线维持治疗的生存记录。2023SOLO1研究公布了随访结果:在长达7年的随访之后,利普卓组的中位OS仍未达到,相比安慰剂组的75.2个月展现出了显著的优势(HR=0.55;95% CI:0.40 ~ 0.76;P=0.0004);7年OS率达67%,远远高于安慰剂组的46.5%。利普卓组中位从随机分配到首次后续治疗或死亡的时间(TFST)为64.0个月,相较安慰剂组(15.1个月)延长超过4年。并且在长达7年的随访过程中,没有发现新的不良事件信号[5]。SOLO1研究结果表明,利普卓是BRCA突变晚期卵巢癌患者实现长期生存安全性良好、有效的治疗选择。
利普卓在BRCA突变晚期卵巢癌一线维持治疗中为患者带来了临床获益,PARP抑制剂以其独特的“合成致死”效应阻断肿瘤细胞的DNA单链修复,最终导致细胞凋亡。在卵巢癌患者中,HRD阳性人群占比约为50%[2],这类患者也是合成致死机制的潜在获益人群。PARP抑制剂维持治疗方案可否使该类患者获益?PAOLA-1研究应运而生。
PAOLA-1是一项多中心、随机对照、双盲的III期临床研究,纳入806例接受含铂化疗联合贝伐珠单抗后达缓解的新诊断晚期卵巢癌患者,以2:1比例随机接受利普卓+贝伐珠单抗或安慰剂+贝伐珠单抗维持治疗,旨在评估利普卓+贝伐珠单抗一线维持治疗的疗效与安全性(图1)[6]。
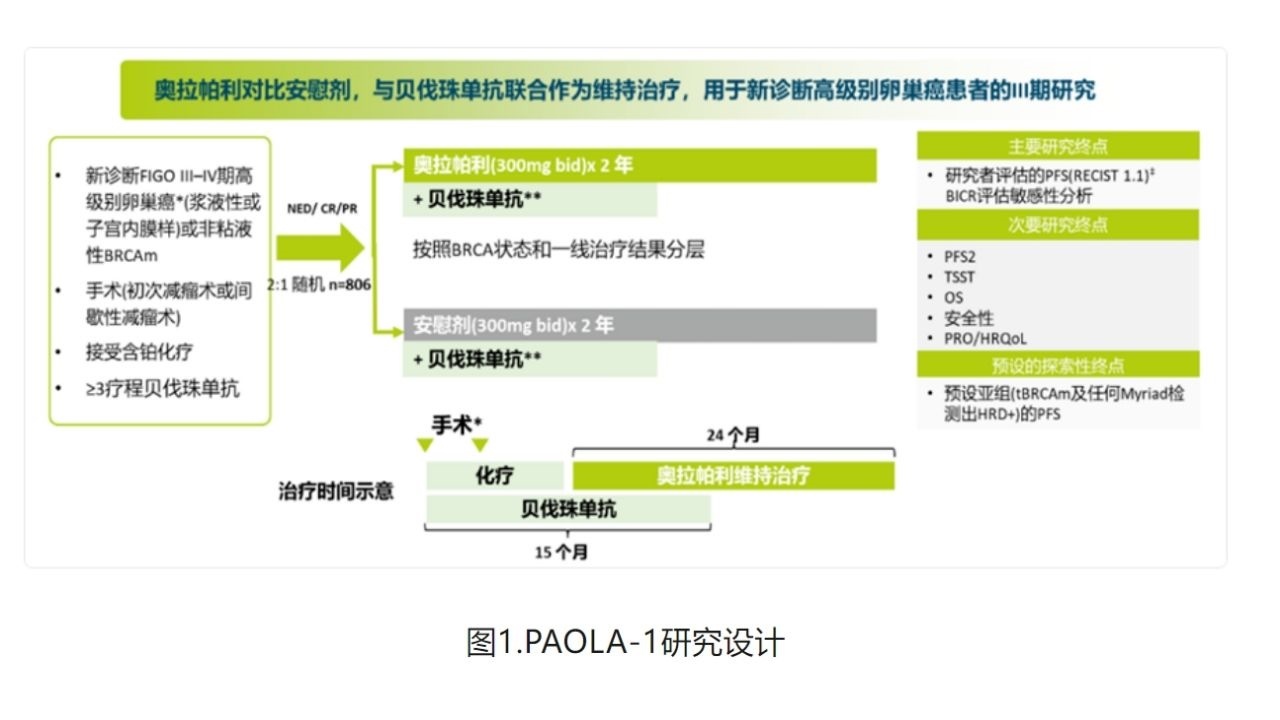
PAOLA-1研究首次亮相于2019年ESMO大会,并随后登上顶刊《新英格兰医学杂志》。结果显示,利普卓+贝伐珠单抗一线维持治疗可显著延长HRD阳性患者患者的中位PFS[6]。此后,PAOLA-1研究长期随访结果在2022年ESMO大会以LBA的形式重磅发布[8],并且研究全文于2023年5月在国际肿瘤学权威杂志《肿瘤学年鉴》(Annals of Oncology)(IF=51.769)正式在线发表,利普卓+贝伐珠单抗一线维持治疗为HRD阳性晚期卵巢癌患者带来PFS和OS双重获益,再次彰显了利普卓的超强实力[7]。
1.利普卓+贝伐珠单抗一线维持,5年OS率高达65.5%,中位OS长达75.2个月
PAOLA-1研究超过5年的随访发现,利普卓联合贝伐珠单抗一线维持治疗HRD阳性患者,尽管安慰剂组中有50%的患者在疾病进展后接受了PARP抑制剂,但利普卓+贝伐珠单抗组依然展现出OS获益。利普卓+贝伐珠单抗组的中位OS达75.2个月,较安慰剂组(57.3个月)延长了近18个月;5年OS率高达65.5%,较安慰剂组提升了17%,死亡风险降低38%(HR=0.62,95%CI 0.45~0.85)(图2)。
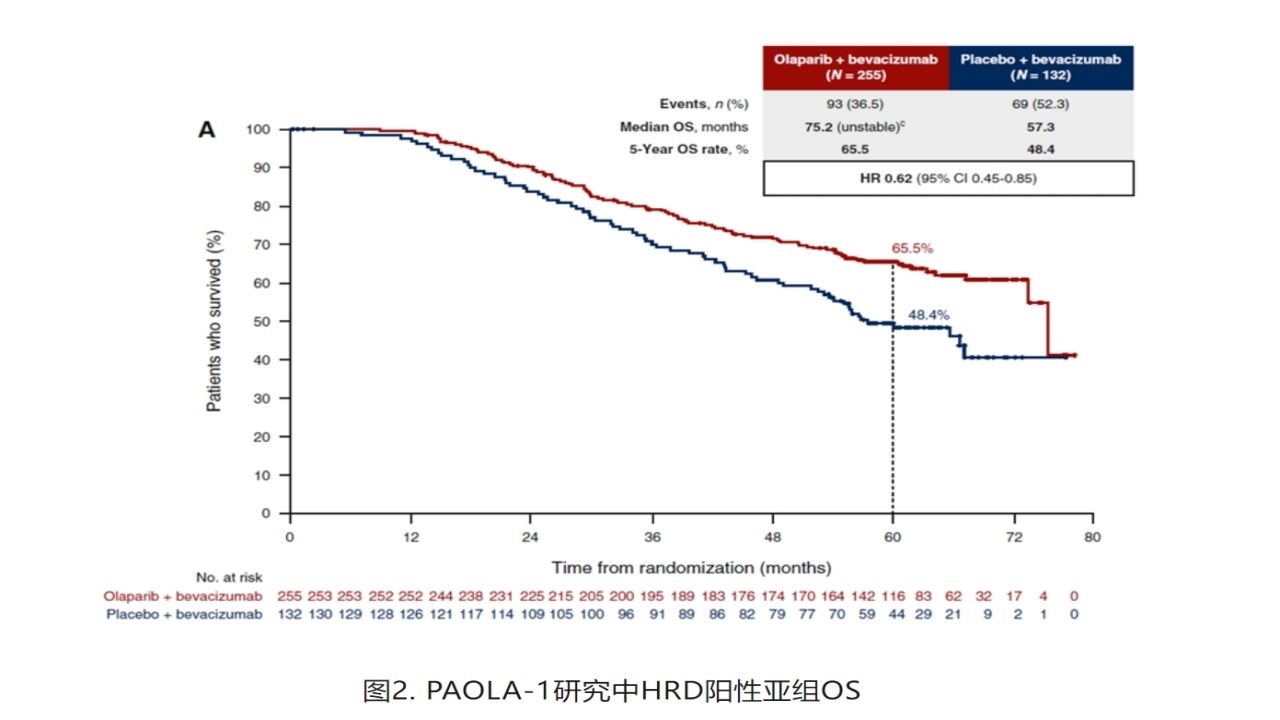
而且,不管患者是否有BRCA突变,利普卓+贝伐珠单抗组都可观察到临床意义的OS获益。在HRD阳性/BRCA突变患者中,利普卓+贝伐珠单抗改善了OS(75.2个月 vs. 66.9个月,HR=0.60,95%CI 0.39~0.93);而在非BRCA突变的HRD阳性患者中,利普卓+贝伐珠单抗组OS也得到了改善(NR vs. 52个月,HR=0.71,95%CI 0.45~1.13)。
2.利普卓联合贝伐珠单抗一线维持,中位PFS长达46.8个月
本次更新的PFS数据显示,在HRD阳性患者中,利普卓+贝伐珠单抗组的中位PFS较安慰剂组明显延长(46.8个月 vs. 17.6个月),降低疾病进展或死亡风险59%(HR=0.41,95%CI 0.32~0.54);5年时未进展的患者比例也明显更高(46.1% vs. 19.2%)(图3)。
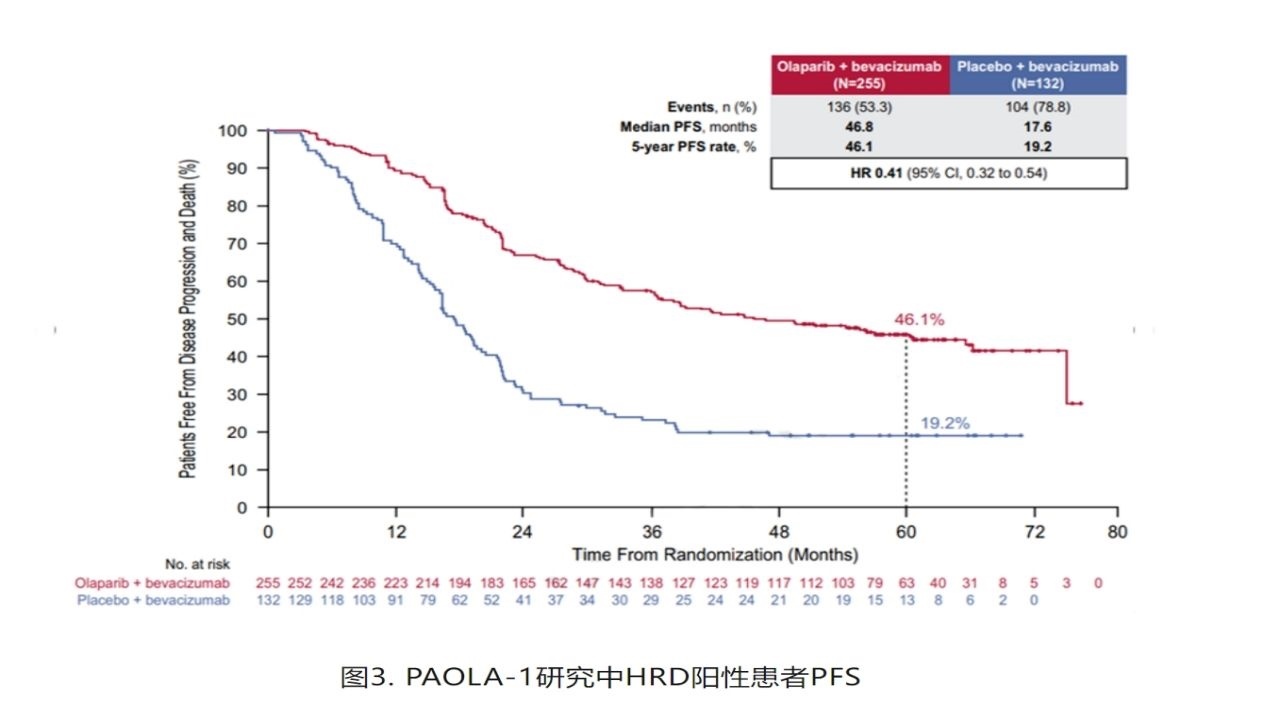
而且,PAOLA-1研究在中位超过5年的随访过程中,未观察到新的安全性信号。
基于PAOLA-1研究的突破性结果,2022年9月14日,中国国家药监局(NMPA)批准PAOLA-1适应症,即利普卓联合贝伐珠单抗用于HRD阳性的晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在一线含铂化疗联合贝伐珠单抗治疗达到完全缓解或部分缓解后的维持治疗。
随着PAOLA-1适应症的获批,使利普卓一线维持治疗获益人群从携带BRCA突变的患者拓宽到更广泛的HRD阳性患者,为超一半初治晚期卵巢癌患者点燃了治愈的希望。在临床实践中,除了疗效外,治疗费用也是药物选择的重要考量因素。因此如何在保证患者最大程度生存获益的同时,降低治疗费用、减轻家庭经济负担,是医患双方关注的重点。利普卓PAOLA-1适应症在获批1年后就成功纳入国家医保目录,无疑是对HRD阳性患者的巨大福音,这意味着药物可及性极大地提升,将使更多卵巢癌患者有机会从利普卓治疗中获益,迎来长期生存的希望和曙光。
文章来源: 逸仙妇瘤专业版
