每周一课|山东大学第二医院妇科系列公开课(第二轮)
编者按:宫颈癌是最常见的妇科恶性肿瘤,且近年来其发病有年轻化的趋势,给社会和家庭带来了严重的疾病负担。宫颈癌在治疗上,采用以手术和放疗为主、化疗为辅的综合治疗方案。但是对于手术方式的选择,即开腹手术和腹腔镜手术孰优孰劣的问题,一直以来颇有争议。其中对于早期宫颈癌腹腔镜手术无瘤操作的问题是焦点之一。在山东大学第二医院妇科系列公开课上朱琳教授就《早期宫颈癌腹腔镜手术无瘤操作的改进探索》这一问题进行了讲解,快来围观吧!
一、研究现状
2018年新英格兰杂志上的两篇文章震惊了整个妇产科学界。
1、第一篇文章是一项回顾性研究,对来源于美国国家数据库的宫颈癌IA2和IB1的患者就腹腔镜和开腹手术结果进行了分析。

图1对来源于美国国家数据库的宫颈癌IA2和IB1的患者的回顾性研究
结果:所有患者均为IA2或IB1期。中位随访时间45个月,1225/2461行微创手术(腹腔镜+机器人),4年病死率9.1%(94/1225);1236/2461行开腹手术,4年病死率5.3%(70/1236)。其他指标:术后90天内死亡:微创组1人,开腹组3人。淋巴结转移率,宫旁浸润情况,切缘情况,术后放化疗情况均无统计学意义。
结论:IA2或IB1期宫颈癌患者行根治性手术时,微创手术会导致生存期下降。
2、另一篇文章是Ramirez教授牵头的一项全球性多中心的前瞻性研究。

图2Ramirez教授牵头的全球性多中心的前瞻性研究
结果:319微创组,312开腹组。两组患者一般资料、病理、肿瘤分期等均无统计学差异。4.5年无瘤生存率:微创组86%,开腹组96.5%。3年无瘤生存率,微创组91.2%,开腹组97.1%。3年总生存率,微创组93.8%,开腹组99.0%。
结论:早期宫颈癌患者,微创手术组无瘤生存期和总生存期均低于开腹手术组。
二、是什么原因导致的上述结果?
LRH&RH的不同之处:
LRH:CO2气腹;
举宫器举宫;
暴露式离断阴道;
宫旁处理:分层、凝切;
标本取出:装袋或裸放;
术毕处理:冲洗液。
RH:拉钩开放式;
钳夹两侧宫角提拉;
大直角钳钳夹阴道;
宫旁处理:大块、缝扎;
标本取出:随即取出;
术毕处理:冲洗液。
三、LHR的改进方法与无瘤技术
(一)阴道离断方式
1、经阴处理:
A、阴道套袖式缝合:先行阴道环切,缝合封闭宫颈,在腹腔镜下处理较容易(阴道狭窄者不宜,操作较困难)。
具体要点包括:
卢戈氏液涂抹宫颈、阴道穹隆及上段,明确着色与不着色的界限;
判断切缘,爱丽丝上下钳夹阴道后壁,注入含垂体后叶素的生理盐水约20ml打水垫,切开并向两侧延伸(切开的长度应尽可能可以放入拉钩),剪水,边分离阴道壁边往上推,可放入拉钩;
同法处理前壁;
用丝线0.5cm间距间断缝合阴道前后壁(从中间向两边缝合),至侧壁时再用电刀切开(注意:此处离输尿管较近,不用过度地使用电凝),缝合;
手推前后间隙,填塞干纱布压迫止血,放入自制阴道塞。
B、先腹腔镜处理阴道前后壁及宫旁,再经阴处理,常内外难一致。
2、腹腔镜下环扎、套扎环:
环扎:在腹腔镜下将宫旁、阴道旁都处理完,用1号可吸收线从两边进行缝合(注意不要穿透阴道壁,以免接触到肿瘤组织),尽可能扎紧,之后可以直接用超声刀切割,大大减少了出血,但缝线缝扎处理后的阴道,很难将阴道封闭,不能完全避免肿瘤组织从缝扎的间隙流出。
套扎圈/套扎器:没有专用的。
3、切割闭合器:
优点:阴道封闭牢靠;
缺点:两端都闭合,取标本还要把封闭的远端切除再缝起来,设备贵,非专用。
(二)举宫方式——改举宫为提拉/牵拉
1、弃用举宫器:
各种举宫器(特别是杯状举宫器)、操作杆,对宫颈、阴道穹隆、颈管及宫腔都有挤压、损伤。
2、子宫悬吊、提拉——各种方法:
缝合宫底/缝扎两侧宫角等,耻上再穿刺,用针持提拉。
我院做法
1、先切除双附件,高位结扎卵巢血管(保留卵巢者切输卵管,游离卵巢血管);
2、直针穿过两侧阔韧带,悬吊子宫,(暴露背侧,切除淋巴、骶韧带及宫旁);目的是不要让子宫两侧的组织干扰术者操作。把1号或0号可吸收线的针掰直,经腹壁将子宫悬吊起来,能很好地暴露子宫背侧,有利于淋巴结清扫、宫旁的处理、阴道后壁的处理和打开阴道直肠间隙,能更清楚地暴露血管与淋巴结。盆腔淋巴结分为两段来清扫,以闭孔神经为界限,切除淋巴时先切闭孔神经内侧再切闭孔神经外侧,能更清晰地暴露术野,方便淋巴结清扫。打开阴道直肠侧间隙时要把输尿管游离开,如果要保留神经,应尽可能靠近骶韧带分离,具体要根据病人临床分期来进行。然后切除骶韧带。
3、打开膀胱反折腹膜,悬吊膀胱(暴露腹侧);打开膀胱反折腹膜后,把原来的针退下再吊起膀胱反折腹膜,可以更好的暴露膀胱和阴道之间的间隙。
切断圆韧带,套住宫体,自穿刺孔分别向两侧牵拉(暴露侧方,处理宫旁)。用粗的不可吸收线(如5号线,在有力牵拉子宫的同时可减小对组织的切割作用)穿过宫体,处理右侧时往左侧拉,处理左侧时往右侧拉,既可以减少打孔,又能很好地暴露宫旁。
(三)标本放袋
1、淋巴结整块切除,切下一个部位,随即放入袋中,避免遗漏或细胞脱落;
2、切除的子宫最好放入取物袋;
3、认真检查切下标本。
(四)术毕盆腔冲洗
一般为温盐水/蒸馏水(43度,3000ml)反复冲洗;
含顺铂或洛铂的生理盐水冲洗盆腔(目前尚有有争议)。
检查切除标本,切除范围完全达到要求:
(五)手术范围,特别是宫旁切除范围——是宫颈癌患者结局最重要的环节
手术范围的大与小是相对的;
对肿瘤组织最大范围的切除与对正常组织最大程度的保护是矛盾的,也是手术的理想状态;
达到理想手术的依据是:
1、宫颈癌的临床分期:

表1宫颈癌国际妇产科联盟(FIGO)分期(2018)
2、手术分型(切除范围):
子宫切除术的分型:
Piver分型:Piver-Rutledge-Smith分型是1974年将根治性子宫切除术分成5类。
Q-M分型:Querleu及Morrow在2007年日本东京的国际会议上讨论并于2008年发表的根治性子宫切除术的分类方法。分为ABCD四型。
Q-M分型更新版:2017年修订,纳入Cibola等的三维化内容(腹侧、侧方、背侧)。
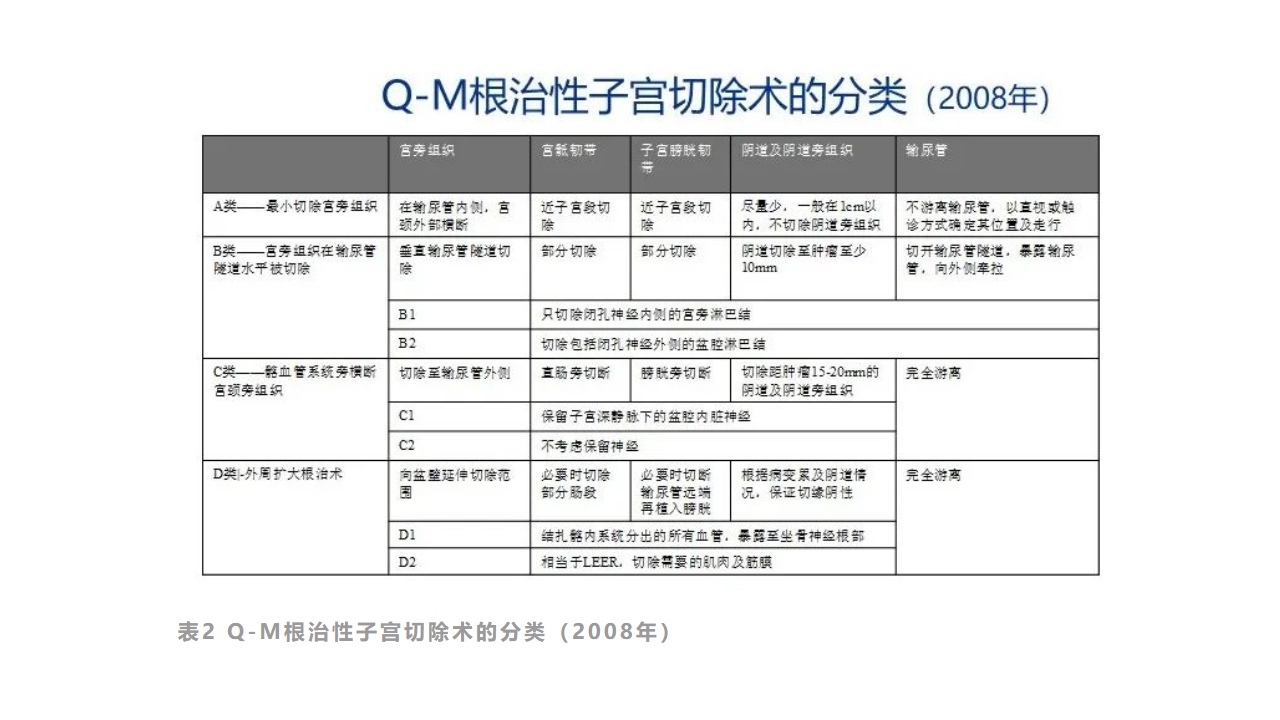
表2Q-M根治性子宫切除术的分类(2008年)

表3Q-M分型更新版(更改点)
四、无瘤技术改进后的手术体会
1,解剖间隙更自然清晰,更体现Cibola三维概念;
2,淋巴结切除的视野清晰;
3,直肠阴道间隙与膀胱阴道间隙分离更容易;
4,膀胱宫颈韧带前后叶间隙清楚;
5,宫旁组织暴露更清晰,切除更容易;
6,整体降低了手术难度;
7,符合无瘤原则。
在处理间隙时我们可以发现在打开阴道直肠间隙后很容易分离阴道壁,打开膀胱反折腹膜后下推膀胱也变得容易很多;由于没有使用举宫装置,宫旁组织、血管、解剖间隙都非常清晰;打开膀胱阴道间隙时也更容易。
在宫旁的处理上,膀胱宫颈韧带的前叶一定要在靠近膀胱的位置上切断,宫旁子宫浅静脉等暴露清晰,超声刀即可凝闭,可以减少双极造成的热损伤,切除膀胱宫颈韧带前叶后分离输尿管子宫间的间隙,暴露膀胱宫颈韧带的后叶,找到子宫深静脉及分支,注意尽量要在完全凝闭血管后再去切除。在C2型手术中,切断主韧带时要紧贴盆壁切除,可以先用双极把血管凝一下再用超声刀切除。
由此可以看到改进后的早期宫颈癌腹腔镜下子宫切除手术通过不举宫等措施体现了无瘤原则,更好的暴露术野也降低了手术难度,也给患者带来了更好的预后。相信腹腔镜手术在宫颈癌手术中仍然能发挥其重要的作用。
[声明:本网站所有内容,凡未注明来源为“转载”,版权均归巢内网所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:巢内网”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们]




