每周一课|山东大学第二医院妇科系列公开课(第二轮)
我国约1.6亿绝经女性,并以每年2%的速度递增,到2030年这一数字将增加至2.3亿。中国女性预期寿命为80.88岁,平均绝经年龄在49.5岁,80%的女性绝经年龄在44~54岁,绝经期占据了女性一生的1/3。
数据统计,我国女性人乳头瘤病毒(HPV)的感染多发于15~24岁及40岁以上年龄段,宫颈癌发病年龄在55~60岁,为高发年龄组,死亡率在85岁左右达到高峰。
有文献报道,大约20%的宫颈癌发生在65岁以上的患者身上[2019年美国阴道镜和子宫颈病理学会(ASCCP)指南特殊人群]。值得注意的是,绝经期女性已经失去注射HPV疫苗预防宫颈癌的机会。
一、宫颈筛查
目前,我国宫颈癌筛查三个阶梯:(1)初筛:液基薄层细胞检测(TCT)+高位HPV;(2)初筛阳性后,转诊阴道镜检查;(3)组织病理检查(确诊的金标准)。每个绝经期女性在不同的阶段都会遇到不同的问题。
1、国内外宫颈癌筛查指南差异
2020年7月30日,美国癌症协会(ACS)制定最新版宫颈癌筛查指南推荐:
(1)年龄<25岁,不需筛查;
(2)年龄在25~65岁:①做初级HPV监测(5年/次)(推荐);②TCT+HPV(5年/次)或TCT(每3年/次)(可接受);
(3)年龄>65岁:既往10年内,连续3次TCT为阴性,或连续2次联合筛查结果为阴性,最近一次检查在3~5年内,若没有过去的筛查记录则应继续筛查,指导达到以上标准;
(4)全子宫切除术后:①过去25年中没有宫颈上皮内病变二级(CIN2)及以上病变的女性,无需筛查;②如果患者已切除子宫或宫颈,且无宫颈高级别鳞状上皮内病变(HSIL)、原位腺癌或癌症病史,可停止筛查;
(5)接种HPV疫苗者,与未接种相同。
我国首部《子宫颈癌综合防控指南》(国家卫生计生委妇幼健康服务司指导、中华预防医学会妇女保健分会组织编写,2017年7月出版)指出:
(1)年龄<25岁:不筛查;
(2)年龄在25~29岁:进行细胞学筛查,结果阴性,每3年筛查一次;
(3)年龄在30~64岁:①HPV和细胞学联合筛查:双阴结果,每5年筛查一次;②细胞学筛查:结果阴性,每3年筛查一次;③HPV筛查:HPV阴性,每3~5年筛查一次;④醋酸染色肉眼观察法(VIA)筛查:阴性,每2年复查一次;
(4)年龄≥65岁:过去10年筛查结果阴性,无CIN病史,终止筛查。
2、初筛方法的选择
以前,宫颈癌的筛查方式主要以TCT为主。随着HPV筛查地位的上升,目前在宫颈癌的筛查多采用TCT+HPV双筛的模式。2019年的ASCCP指南进一步强调了HPV在筛查过程中的重要地位,作为基于HPV筛查基础上的风险评估。
因此,对于不同年龄的人群将选择不同的初筛方法:对于年龄>25岁的女性,推荐TCT+HPV的联合筛查模式;年龄<25岁的女性及妊娠期,推荐细胞学筛查。

图1TCT筛查效果低于HPV筛查(源自2019年ASCCP指南)
3、TCT涂片的评估
评估TCT涂片时,应注意以下几点:
(1)不论是TCT还是HPV,均已宫颈脱落细胞为检测对象。
(2)足够的鳞状细胞数量:液基薄层细胞涂片≥5000个保存良好的清晰的鳞状上皮细胞;绝经后妇女的细胞数量标准≥2000个(TBS报告系统2014版)。对于绝经患者如何取得满意的脱落细胞来作为检测对象,值得我们探讨。绝经后的女性脱落细胞量会减少,为保证获得充足的细胞量进行切片评估,取样时需适度增加旋转圈数。例如图2,该病例病理诊断显示:未见上皮内病变或恶性病变,同时备注“有宫内膜细胞,患者>45岁”,提示我们需要关注患者子宫内膜相关问题,需要做B超进一步检查以及询问患者是否有异常出血问题。
(3)颈管及移行区成分:对于绝经女性,有些会出现颈管粘连,这种情况下需要扩宫颈取颈管内脱落细胞,同时重视这类人群是否出现隐匿性的颈管相关病灶,尤其是宫颈腺上皮病变的出现。
(4)结果判读:正常鳞状上皮细胞(NILM)、非典型鳞状上皮细胞不能明确意义细胞(ASCUS)、低度鳞状上皮内病变(LSIL)、非典型鳞状上皮细胞-不除外高度鳞状上皮内病变细胞(ASCH)、高度鳞状上皮内病变(HSIL)、鳞状上皮细胞癌(SCC)、非典型腺细胞(AGC)、宫颈原位腺癌(AIS)。对于结果的判读,分为两个区域,分为低危细胞学结果和高危细胞学结果,界限在于LSIL和ASC-H之间。对于ASC-H以上的诊断结果,需要特别注意的是,无论HPV是阴性还是阳性,都需要转诊阴道镜检查。
4、取样中的困难及解决方案
取样过程中遇到的问题有:(1)患者筛查意识淡薄,主动自愿筛查人数少;(2)脱落细胞数量少,行宫颈TCT及HPV检查取材困难(2019ASCCP指南同时强调同一标本同一实验室进行检查,避免召回HPV阳性患者再次检查,因此采取双筛模式);(3)穹隆缩短或颈管粘连,颈管内细胞无法取到,尤其是宫颈锥切术后;(4)阅片困难,经常出现ASCUS的结果。
针对这些问题,可能的解决方案包括:(1)加强宣教。无论从经济学角度还是从自身健康角度,疾病的管理重在预防,具有事半功倍的效果。(2)取材前大棉签轻擦宫颈的血迹或分泌物。(3)避免使用润滑剂。润滑剂不仅影响图片质量且影响取材,如遇阴道干涩可用水剂起到润滑效果。(4)取样时增加刷取圈数,以获取更多的脱落细胞。(5)对于颈管粘连(包括宫颈病变治疗后随诊)的绝经女性,需要扩张宫颈,以期获得足量的颈管细胞。(6)对于不满意标本的处理:在2~4个月后,重复TCT检查。(TBS报告系统2014版)
5、阴道镜检查
妇科医生应该重视对患者的初步检查,对于绝经女性宫颈筛查建议做TCT和HPV检测双筛,对于双筛结果异常者做阴道镜检查。
(1)阴道镜检查的主要指征:①异常或不确定的宫颈癌筛查结果。临床中需要关注更多的指南和共识,以及对患者的随诊不断的进行总结;②提示宫颈癌的症状或体征,包括盆腔检查时发现任何可疑的宫颈异常,异常生殖道出血,或原因不明的宫颈阴道分泌物;③下生殖道癌前病变治疗后的随访。
(2)阴道镜检查禁忌证:阴道镜检查无绝对禁忌证;患有急性生殖道感染时应在纠正炎症后再行检查;可在月经周期的任何时间进行阴道镜检查,但无特殊情况不建议在月经期检查。
(3)阴道镜检查及活检中的困难:①雌激素缺乏,阴道萎缩,弹性降低,表皮变薄,甚至会形成穹隆部的缩窄环,造成暴露困难,且极易损伤出血。②雌激素缺乏,鳞柱交界内移,可能病灶隐匿颈管内,阴道镜下不易发现引起漏诊。③阴道镜检查过程中,患者的不适感觉加重,配合难度增大,延长了阴道镜检查时间。④宫颈上皮变薄,醋酸白上皮与病变严重程度不符;上皮细胞中糖原含量减少,碘染色不均或无法染色。⑤活检困难:宫颈变硬,标本深度不够。
生育期女性阴道:生育期女性阴道1型转化区红润,颜色为粉红色,皱襞较多,阴道有弹性,阴道镜检查相对容易操作。
不典型的白上皮:绝经女性阴道黏膜极易受伤,老年性阴道炎有充血表现,粘膜皱襞消失,阴道镜检查较困难,甚至让患者感到不适。患者阴道镜检查显示3型转化区,宫颈因反复宫颈检查操作有出血表现,甚至上皮卷曲,白上皮不典型,上皮极易脱失。滤光之后可见点状血管,碘实验后无法分清成熟鳞状上皮细胞和非成熟鳞状上皮细胞,不易分清病灶区域。
隐匿的白上皮:患者阴道镜检查显示3型转化区,颈管后唇有厚白上皮,认定为高级别病变的表现,涂抹醋酸以及碘实验后上皮卷曲以及极易缺失。该患者TCT检查为HSIL,HPV筛查为阴性,宫颈管搔刮术(ECC)结果为CIN3累腺,该病例为HPV阴性癌前病变的结果。因此,绝经后女性患者应增加ECC检查,避免漏诊。
(4)解决方案:①局部应用雌激素,改善绝经后女性阴道萎缩,改善鳞状上皮的厚度及阴道的微生态的环境,使阴道镜检查的不适度降低,提高阴道镜检查质量。②阴道镜检查过程中操作轻柔。③对于阴道镜检查中任何异常情况,均应活检证实;对于高风险的初筛结果与阴道镜检查图像不符时,建议增加ECC,减少漏诊率。④宫颈活检注意活检深度,建议使用锐利的活检钳。⑤如无症状阴道萎缩患者需要进行阴道镜检查,应用以上方法(局部雌激素)治疗3周,即可显著改善阴道镜检查的质量,以充分评估阴道或子宫颈病变的存在。理想情况下,应该在停止用药后数天至一周后再进行阴道镜检查。
二、宫颈病变的治疗
由于宫颈癌前病变可能发展为宫颈癌,因此所有确诊的患者都应及早接受治疗。其治疗难点和解决方案主要体现在以下几方面内容:
1、治疗难点
(1)雌激素水平的降低,阴道萎缩,弹性降低,宫颈萎缩或宫颈暴露困难,锥切困难。
(2)阴道穹隆部膨出,误认为宫颈,宫颈锥切损伤临近器官组织。
(3)因鳞柱交界内移,颈管内病灶多见且较深,锥切深度较难把控,内切缘病灶残留率升高。
(4)需要指出的是:如果能进行锥切,应避免直接切除子宫(2019年ASCCP指南)。
2、解决方案
(1)锥切前做一定阴道镜评估,确定转化区类型及病变区域和范围,尤其要确定穹隆及宫颈的边界。
(2)治疗炎症,减少术中出血。
(3)国际宫颈病理与阴道镜联盟(IFCPC)在规范阴道镜术语中,切除3型转化区,此方法切除组织比较多,包括相当一部分宫颈管组织,治疗深度为15~25mm。
(4)术前B超检查,评估颈管长度,以及确定最大切除深度。
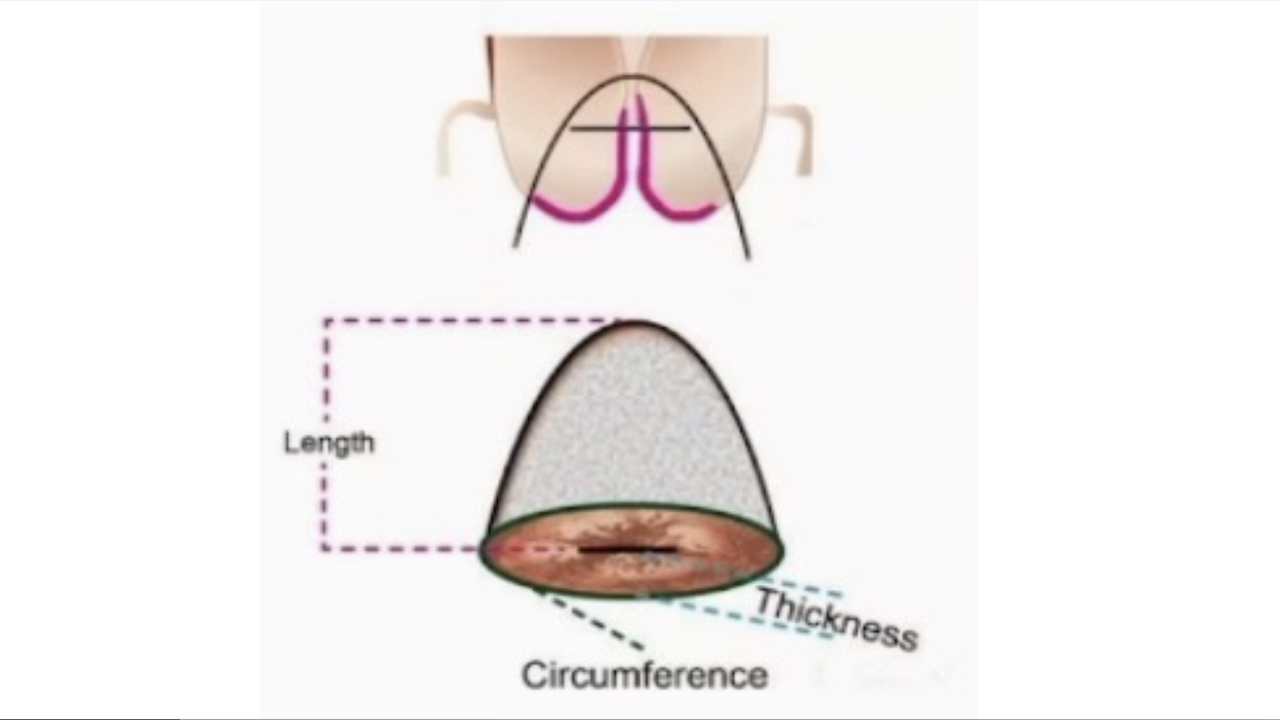
图2锥切手术示意图
三、宫颈异常的随诊
1、随诊难度
随诊的难度主要体现在:
(1)患者自身和阴道局部免疫力的降低,阴道微环境异常,HPV转阴率降低。
(2)持续HPV阳性,加上更年期心理变化,更易产生焦虑症状,而且担心会传染家人,影响睡眠而进一步降低抗病力。
(3)曾经的就医过程,产生的外阴阴道的不适感,害怕复诊。
(4)筛查异常后的随诊监测持续时间过长:①对于高级别病变治疗后患者,术后6个月随诊,检查结果若为阴性,则改为1年监测一次,直到连续出现3次阴性结果,进而更改为每3年随诊一次,至少随诊25年。随着时间的推移,随诊也越来越困难。
(5)锥切后产生颈管粘连,随诊是难上加难,“不切担心,切了让随诊难上加难更担心。”
2、解决方案
(1)舒缓患者焦虑情绪,调整睡眠,改变不良习惯,指导性生活,并建立长期随诊意向。
(2)对于术后仍持续HPV感染的患者,可应用改善阴道微环境的药物,积极治疗老年性阴道炎,增加局部抗HPV的能力。
(3)建立长期随诊计划,避免短期内的重复筛查。
(4)掌握好锥切指征,做到留有随访余地,积极处理颈管粘连。
(5)对于锥切切缘阴性、术后持续HPV阳性的患者,如果没有继续发现高级别病变和HPV相关的外阴阴道疾病,需要对术后HPV持续不转阴患者“宽容”一些,从患者的症状、三阶梯筛查以及B超三种方式进行筛查,做好后期评估,而不是再次进行手术切除。
四、小结
绝经后女性因雌激素缺乏,易引起生理和心理的变化,尤其是下生殖道的变化,使筛查变得困难重重。针对雌激素缺乏,临床上通常采用局部应用雌激素软膏或阴道胶囊,既可改善阴道微环境来增加抗HPV能力,也可改善筛查过程中的不适感,让患者能够坚持筛查。
同时,由于绝经后女性病变的隐匿性和不典型性,必须结合病史综合评估风险,筛出高风险人群进行规范治疗。此外,尽早处理宫颈及阴道壁的粘连,让随诊能更好的持续下去。在管理过程中,对绝经的这类人群,做到有爱心,细心的查找疾病,随诊过程中做的有耐心,医护自己有信心、恒心、责任心,会起到事半功倍的效果。
[声明:本网站所有内容,凡未注明来源为“转载”,版权均归巢内网所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:巢内网”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们]






